某兴趣小组利用氯酸钾和二氧化锰共热来制取一定量的氧气.将2g二氧化锰与一定量氯酸钾共热到产生9.6g的氧气后,便停止加热,此时测得剩余固体中二氧化锰的质量分数为10%.求:(1)生成氯化钾多少g?______(2)反应前总的氯酸钾的质量是多少g?______.
【答案】
分析:某兴趣小组利用氯酸钾和二氧化锰共热来制取一定量的氧气.将2g二氧化锰与一定量氯酸钾共热到产生9.6g的氧气后,便停止加热,此时测得剩余固体中二氧化锰的质量分数为10%.求:
(1)根据化学方程式,已知氧气的质量,可求生成氯化钾的质量、参加反应的氯酸钾的质量;(2)已知“2g二氧化锰”、“测得剩余固体中二氧化锰的质量分数为10%”,可求剩余氯酸钾的质量,则反应前总的氯酸钾的质量为参加反应的氯酸钾的质量和剩余氯酸钾的质量之和.
解答:解:(1)根据化学方程式,已知氧气的质量,可设参加反应的氯酸钾的质量是X,生成氯化钾的质量为Y.
2KClO
3
2KCl+3O
2↑
245 149 96
x y 9.6g
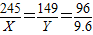
解得:x=24.5g,y=14.9g
则:(1)生成氯化钾的质量14.9g
(2)反应前总的氯酸钾的质量 2g÷10%-2g-14.9g+24.5g=27.6g
故答为:(1)14.9g;(2)27.6g
点评:本题是运用化学中的基本思想质量守恒思想,掌握利用化学方程式计算的方法和步骤.

 2KCl+3O2↑
2KCl+3O2↑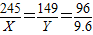


 名校课堂系列答案
名校课堂系列答案