
分析 分析所发生的反应,可发现反应后总质量减轻是由于生成了气体二氧化碳,根据质量守恒定律可求出二氧化碳的质量.然后利用二氧化碳的质量,根据反应的化学方程式,计算恰好完全反应时碳酸钙的质量,最后使用质量分数的计算公式,求出样品中碳酸钙的质量分数.
解答 解:(1)生成二氧化碳的质量为:12.5g-8.1g=4.4g;
(2)设碳酸钙的质量为x.
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 44
x 4.4 g
$\frac{100}{x}$=$\frac{44}{4.4g}$
x=10 g
石灰石样品中碳酸钙的质量分数为:$\frac{10g}{12.5g}$×100%=80%
答:石灰石样品中碳酸钙的质量分数是80%.
故答案为:(1)4.4;
(2)80%.
点评 根据反应的化学方程式能表示反应中各物质的质量关系,由反应中某物质的质量可计算出反应中其它物质的质量.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:初中化学 来源: 题型:选择题
| A. | 用5%的双氧水制氧气是为了避免反应过快 | |
| B. | 用36.5%的浓盐酸制得的二氧化碳更纯净 | |
| C. | 用98%浓硫酸检测金属的活动顺序更准确 | |
| D. | 用100%纯净水电解才能准确测定水的组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
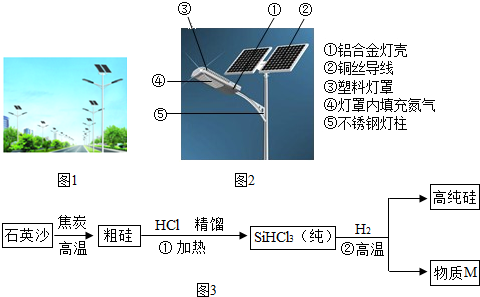
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com