
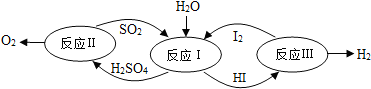
分析 (1)根据反应I为二氧化硫与碘发生氧化还原反应生成硫酸和HI进行分析;
(2)根据单质中元素的化合价为零分析;
(3)根据质量守恒定律分析解答.
解答 解:(1)由图可知,反应I为二氧化硫与碘发生氧化还原反应生成硫酸和HI,该故答案为:SO2+2H2O+I2=H2SO4+2HI;
(2)反应Ⅲ中,H和I由化合态变为游离态,元素的化合价发生了改变;
(3)反应I的化学方程式为:SO2+2H2O+I2$\frac{\underline{\;太阳能\;}}{\;}$H2SO4+2HI,根据质量守恒定律可知,制得H2中氢元素最初来源于水;
故答案为:(1)SO2+2H2O+I2$\frac{\underline{\;太阳能\;}}{\;}$H2SO4+2HI;(2)H;I;(3)H2O.
点评 本题考查化学方程式的书写,元素的化合价等知识,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 供给的氧气减少 | B. | 供给的氧气增加 | ||
| C. | 使温度降到火柴棍的着火点以下 | D. | 使火柴棍的着火点降低 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 可用肥皂水区别硬水和软水 | |
| B. | H2O是由一个氢分子和一个氧原子构成 | |
| C. | H2O中氧元素的化合价为-2 | |
| D. | H2O是氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
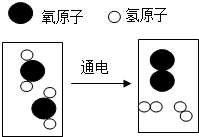 在物质的宏观性质、微观组成(或结构)和表示符号之间建立联系是化学学科的特点.某化学反应的微观示意图(表示氧原子,表示氢原子)如图:
在物质的宏观性质、微观组成(或结构)和表示符号之间建立联系是化学学科的特点.某化学反应的微观示意图(表示氧原子,表示氢原子)如图:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
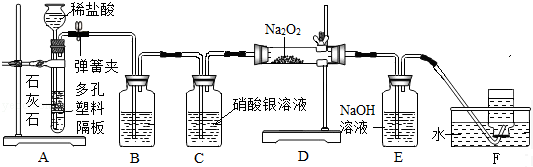
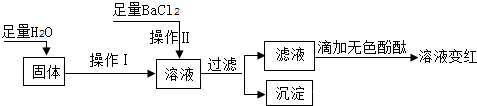
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com