
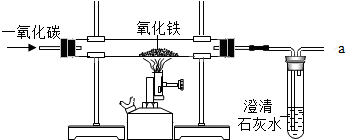
 钢铁的冶炼是我国古代的化学工艺,请你参与到以下炼铁的实验中探究(一)炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置见图,对实验进行分析并回答:
钢铁的冶炼是我国古代的化学工艺,请你参与到以下炼铁的实验中探究(一)炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置见图,对实验进行分析并回答:分析 (1)酒精灯火焰中,外焰温度最高;
(2)高温条件下,氧化铁和一氧化碳反应生成铁和二氧化碳;
(3)一氧化碳具有可燃性,与空气或氧气混合达到一定程度时,遇明火会发生爆炸;
(4)一氧化碳燃烧生成二氧化碳;
(5)二氧化碳能使澄清石灰水变浑浊;
除铁粉以外,四氧化三铁、氧化亚铁也是黑色的;
(6)生铁的主要成分是铁,还含有碳等物质;
(7)铁和稀盐酸反应生成氯化亚铁和氢气,根据提供的数据可以进行相关方面的计算.
解答 解:(1)由于酒精喷灯的外焰的温度最高,加热时要用外焰进行加热.
故填:外焰.
(2)一氧化碳还原氧化铁(Fe2O3),主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)由于玻璃管内有空气,通入一氧化碳高温时易发生爆炸,所以实验前先通入CO,排净玻璃管中的空气再开始加热.
故填:先通入CO再开始加热.
(4)为了防止一氧化碳对大气的污染,所以,实验时要在装置末端a处燃着一盏酒精灯除去反应剩余的CO.
故填:防止一氧化碳污染环境.
(5)A、试管中澄清的石灰水变浑浊,证明该反应有二氧化碳生成,该选项说法正确;
B、因此反应也可能生成四氧化三铁或氧化亚铁,它们也是黑色的,所以玻璃管中红色的氧化铁粉末变成黑色,该产物不一定是铁,该选项说法正确;
C、由题意可知,此反应中的生成物可能有铁粉和四氧化三铁、氧化亚铁,所以玻璃管中的固体物质的质量比反应前减少了,证明一定有铁生成的说法是错误的,该选项说法不正确.
故选:C.
(6)用该方法炼出的铁不是生铁,因为生铁是含有碳元素的混合物,而该方法得到的是铁单质.
故填:不是.
(7)设铁的质量为x,氯化氢质量为y,
反应前后的质量差即为反应生成氢气的质量,因此生成氢气的质量为:10g+100g-109.8g=0.2g,
Fe+2HCl═FeCl2+H2↑,
56 73 2
x y 0.2g
$\frac{56}{x}$=$\frac{73}{y}$=$\frac{2}{0.2g}$,
x=5.6g,y=7.3g,
样品中铁的质量分数为:$\frac{5.6g}{10g}$×100%=56%,
稀盐酸的溶质质量分数为:$\frac{7.3g}{100g}$×100%=7.3%,
答:样品中铁的质量分数为56%,稀盐酸的溶质质量分数为7.3%.
点评 本题主要考查一氧化碳与氧化铁反应实验装置、实验现象、一氧化碳的化学性质和污染,属基础性知识考查题.


 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
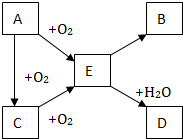 A、B、C、D、E是初中化学中常见的不同物质,其中A为黑色的固体,B为白色的固体,它们之间的转换关系如图箭头所示:
A、B、C、D、E是初中化学中常见的不同物质,其中A为黑色的固体,B为白色的固体,它们之间的转换关系如图箭头所示:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com