
分析 根据图示即可知道仪器的名称;发生装置的选择与反应物的状态和反应条件有关,收集装置的选择与气体的密度和溶解性有关;二氧化碳能溶于水;根据碳酸钙和盐酸的反应计算盐酸的质量分数即可.
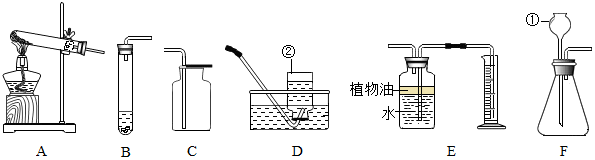
解答 解:(1)据图可以看出,①是长颈漏斗;②是集气瓶,故填:长颈漏斗;集气瓶.
(2)在实验室用高锰酸钾制取氧气,是固体加热型反应,应该选择的发生装置是A,由于氧气的密度大于空气,可以使用向上排空气法收集,氧气不易溶于水,可以使用排水法收集,故应选用的制取装置是AC或AD;加热高锰酸钾分解生成锰酸钾、二氧化锰和氧气,反应的化学方程式是 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.故填:AC或AD;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)要检查F装置的气密性,可以关闭右侧止水夹,往长颈漏斗内注水至漏斗颈内形成一段液柱,一段时间后液面不下降,说明装置气密性良好,故填:关闭右侧止水夹,往长颈漏斗内注水至漏斗颈内形成一段液柱,一段时间后液面不下降,说明装置气密性良好.
(4)由于二氧化碳能溶于水,故使用E装置来测量生成CO2气体的体积,需要在在水面上放一层植物油,是为了防止二氧化碳溶于水,故填:防止二氧化碳溶于水.
(5)②将少量CO2气体通入盛有大量澄清Ca(OH)2溶液的大烧杯中,二氧化碳与氢氧化钙反应生成碳酸钙沉淀,故烧杯中溶液的质量与之前相比会减小,故填:减小.
(6)取12g石灰石(主要成分是CaCO3,杂质不参加反应)放入烧杯中,向其中加入100g一定质量分数的稀盐酸,二者恰好完全反应,反应结束后,称量烧杯中剩余物质的总质量为107.6g(不包括烧杯的质量,且气体溶解忽略不计),则稀盐酸中溶质的质量分数是多少?
根据题干可以看出,产生二氧化碳的质量为:12g+100g-107.6g=4.4g,设盐酸中溶质的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 44
x 4.4g
$\frac{73}{44}=\frac{x}{4.4g}$
x=7.3g
故盐酸中溶质质量分数为:$\frac{7.3g}{100g}×100%$=7.3%
故填:7.3%.
点评 本题考查的是常见的气体的实验室制取的知识,解答本题要注意发生装置的选择与反应物的状态和反应条件有关,收集装置的选择与气体的密度和溶解性有关.


科目:初中化学 来源: 题型:选择题
| A. | 火碱、熟石灰可以敞口放置 | |
| B. | 少量浓硫酸粘在皮肤上,立即涂上碳酸氢钠溶液 | |
| C. | 室内电器着火,先切断电源再灭火 | |
| D. | 可燃物只要露天放置就会燃烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 人体缺少必须微量元素会得病,因此应尽可能多吃含有这些元素的营养补剂 | |
| B. | 用氮气作食品保护气,是利用其化学性质稳定 | |
| C. | 一氧化碳有毒,燃着的煤炉会产生一氧化碳,在煤炉上放一壶水能防止人中毒 | |
| D. | 做饭时,若燃气灶的火焰呈现黄色,锅底出现黑色,则需要调小灶具的进风口 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | HNO3 NaCl Na2CO3 CaCl2 | B. | HCl NaOH CuSO4 MgSO4 | ||
| C. | Na2CO3 K2SO4 BaCl2 HCl | D. | Ba(OH)2 NaCl Na2SO4Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
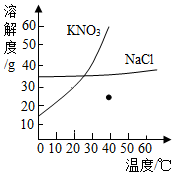 根据给出的KNO3和NaCl两种物质的溶解度表、溶解度曲线,回答问题.
根据给出的KNO3和NaCl两种物质的溶解度表、溶解度曲线,回答问题.| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 温度/℃ | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钙 | 65.0 | 74.5 | 100 | 116 |
| 氯化镁 | 53.8 | 54.8 | 56 | 58 | |
| A. | 氯化镁和氯化钙的溶解度都随着温度的升高而减小 | |
| B. | 10℃时,将54g氯化镁溶于46g水中可配制54%的溶液 | |
| C. | 20℃时,氯化钙的饱和溶液中溶质的质量分数为74.5% | |
| D. | 40℃时,氯化钙和氯化镁的饱和溶液冷却至10℃都有结晶现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
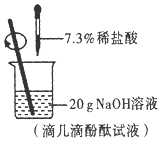 将溶质质量分数为7.3%的稀盐酸滴入盛有20g氢氧化钠溶液(滴有几滴酚酞试液,如图所示)的烧杯中,恰好完全反应时消耗稀盐酸50g.
将溶质质量分数为7.3%的稀盐酸滴入盛有20g氢氧化钠溶液(滴有几滴酚酞试液,如图所示)的烧杯中,恰好完全反应时消耗稀盐酸50g.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 道路洒水,空中喷雾 | |
| B. | 植树造林,绿化环境 | |
| C. | 充分利用化石燃料煤 | |
| D. | 加快地铁建设,减少机动车尾气排放 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com