
����Ŀ���ܽ��������г���������ͬ������ˮ�е��ܽ�������ͬ���±���KNO3��NaCl�ڲ�ͬ�¶��µ��ܽ�ȣ���λ��g/100gˮ����
�¶ȣ��棩 | 0 | 20 | 40 | 60 | 80 | 100 |
KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
��1���ϱ��е�����������40��ʱ��_______���ѧʽ�����ܽ�Ƚϴ�
��2����д��һ�ֽ�KNO3�IJ�������Һת��Ϊ������Һ�ķ���____________________��
��3��20��ʱ����20gNaCl����50gˮ�У�������Һ��������______g��
��4����NaCl��Һ�еõ�NaCl����ķ�����________��
��5�����ñ����е����ݼ���20��ʱ��NaCl������Һ����������_________��
���𰸡�KNO3 ����KNO3�����¶Ȼ������ܼ��� 68 �����ᾧ 26.5%
��������
��1�����ϱ��ɿ������ϱ��е�����������40��ʱ��KNO3���ܽ�Ƚϴ�
��2������KNO3���ܽ�����¶ȵ����߶�����KNO3�IJ�������Һת��Ϊ������Һ�ķ����н����¶ȣ�������KNO3�������ܼ�����
��3��20��ʱ��NaCl���ܽ����36.0g����50gˮ��������ܽ�18gNaCl���ʽ�20gNaCl����50gˮ�У�������Һ��������50g+18g=68g��
��4��NaCl���ܽ�����¶ȱ仯Ӱ�첻�ʴ�NaCl��Һ�еõ�NaCl����ķ����������ᾧ��
��5��20��ʱ��NaCl���ܽ����36.0g����20��ʱ��NaCl������Һ����������Ϊ��![]() ��26.5%
��26.5%



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ѧϰЧ�ʵij��÷���,�����йع�����������ȫ��ȷ����( )
A. ����������һ��������ɵ�,�������һ�ִ�����
B. ���ֽⷴӦ�г����������ˮ����,���г����������ˮ���ɵķ�Ӧ���Ǹ��ֽⷴӦ
C. ����������,����ͨ����������Ŀ���ʴ���ܱ���ǿ
D. ���еú�����������Ӧ�л�������,��ʳ�︯���ǻ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������ܹ�ʵ�����Ӧʵ��Ŀ�ĵ���
A. 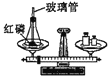 ��֤�����غ㶨��
��֤�����غ㶨��
B. 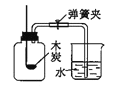 �ⶨ�����������ĺ���
�ⶨ�����������ĺ���
C. 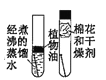 ̽��������ʴ������
̽��������ʴ������
D. 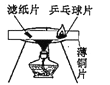 ̽��ȼ�յ�����֮һ���¶ȴﵽ�Ż��
̽��ȼ�յ�����֮һ���¶ȴﵽ�Ż��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ������ȡ���岢�����й�ʵ���װ��ͼ����ش����⣺

��1��ͼ�б�ʶ��������������____��
��2��ʵ������װ��A��ȡ�����Ļ�ѧ����ʽ____��ʵ���Ҽȿ�����ȡCO2���ֿ�����ȡO2�ķ������ռ�װ�����Ϊ____����A~E��ѡ����ʵ������ȡCO2�Ļ�ѧ����ʽΪ____��
��3������Fװ���ռ�һƿ�����ij���壬������������____������ĸ���ţ�
A��NH3 B��H2 C��O2
��4��2018��4��11�գ�����Բ������������ڵġ���ͭ���v��y��ng������Ӣ�����ز�����������������������ɫ��С���������ϵ�֪������ͭ�����ڱ�¶�ڿ�����������ͭ�̣���Ҫ�ɷ�ΪCu2(OH)2CO3��

�ٸ���ͭ�̵ijɷ֣�����Ϊͭ�̵��γ���ͭ��ˮ��������____��ͬ���õĽ����
��Ϊ̽��ͭ�̵�������Ƿ���̼Ԫ�أ�С��ͬѧ������ͭ����ȡ��������ͭ�̣�������װ��A��____������ţ���������ʵ�飬���۲쵽____����֤��ͭ�̵�����к���̼Ԫ�أ�ʵ�����ʱ��Ӧ��___������ţ�A.�Ƴ����ܣ�B.Ϩ��ƾ��ƣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڻ�ѧ��ȤС���У���ʦΪ��ұ���һ����ˮ���𡱵�ħ��������Ƭ���ɵ���֬���м����һЩ����ɫ�����ĩ�����ɡ����ı��ɡ����ý�ͷ�ι����ı��ɡ��ϵ�ˮ�����κ��ı��ɡ�ȼ������������ʦ���ܣ��õ���ɫ����Ϊ�������ƣ�Na2O2��������ˮ��Ӧ����һ�ֳ��������Թ��廯����X��һ�ֳ�������Y��
��������⣩������X������Y�ֱ���ʲô��
���������룩ͬѧ����ΪXӦΪNaOH������Y�ijɷֲ����˷��磬���룺��O2����H2����CO2��
�����ۣ�����_____������ţ��϶���������������_____��
��ʦָ����ͬһ��ѧ��Ӧ�У�����Ԫ�ػ��ϼ۽��ͣ�����Ԫ�ػ��ϼ����ߡ�Na2O2��OԪ���ԡ�1�ۡ�
������Ϲ��ɣ�����Ϊ����Y�Ļ�ѧʽΪ_____��
��ʵ����֤��
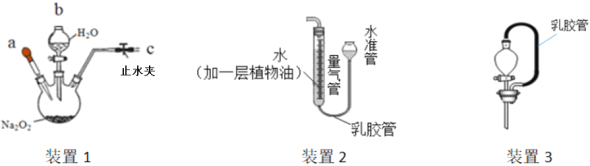
ʵ�鲽�� | ʵ������ | ʵ����� |
�� _____�����Һ©���м�ˮ���� ��Һ©������ | ��Һ©������һ���ȶ���ˮ�� | װ��1���������� |
��ȡ����Na2O2��������ƿ�У���ֹˮ�У���������ˮ | �����ܽ⣬�γ���ɫ��Һ�������ݲ��� | |
�۴�a���ιܵμ�CuSO4��Һ | _____ | XΪNaOH |
д��Na2O2��H2O��Ӧ�Ļ�ѧ����ʽ_____��
���������⣩Na2O2���峨�ڷ���һ��ʱ�����ϸ�ĵ�ͬѧ�������к���������ɫ��ĩ��
���������ϣ�Na2O2�ڿ����п��Ժ�CO2��Ӧ�����ʣ�����Na2CO3��O2��
������̽�����ⶨ��Na2O2��Ʒ��Na2CO3������������
��ȡ5.0g����Ʒ��װ��1�У���ˮ�����Һ����ȴ�����£�
�ڽ�װ��2��װ��1���ӣ���b����Һ©���滻Ϊװ��3����ʢϡ���ᣩ��
�����µ���װ��2��ˮ������������Һ����ƽ,��¼�����Һ�����Ϊ20.0mL��
����װ��3����Һ�еμ�ϡ������_____����ʵ������
���ٴ����µ���װ��2��ˮ������������Һ����ƽ��
��¼�����Һ�����Ϊ80.0mL��
��֪CO2�ڸ�ʵ�黷���µ��ܶ�ԼΪ1.8��10-3g/mL������ʵ�����ݼ��㣺
��1������CO2������Ϊ_____g����������ȷ��0.01����
��2����Na2O2��Ʒ��Na2CO3������������д��������̣�_____��
��ʵ���������װ��3�滻��Һ©�����ŵ���_____��
��ħ�����أ���ˮ���𡱵�ԭ����
����֬���п�ȼ�ԣ�����֬����O2�Ӵ����۴������仯�ĽǶ�Na2O2��H2O�ķ�Ӧ��_____��Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬѧ�Ƿ������ʵ�ƻ��֭�ڿ����з���һ��ʱ�����ɫ���·�������һ�������ǣ��о���С��ͬѧ��Ʋ�����ʵ�飬̽��ƻ��֭��ɫ��ԭ��
���������ϣ�
a��ƻ��֭�к���0.001%�Ķ��������ʣ�ͬʱҲ���ж�������ʣ���ӿ�������е�������Ӧ��Ϊ��ɫ��
b���������ڿ����л���Ũ���ᷴӦ���ܱ�Ϊ��������������������ҺΪ��ɫ
c�����軯�أ�KSCN����Һ��ɫ����
ҩƷ | ��������Һ | ��������Һ |
KSCN��Һ | ����ɫ | ���ɫ |
����������裩
��.ƻ��֭��ɫ��ƻ���е���Ԫ���й�
��.ƻ��֭��ɫ��ƻ��֭�еĶ������������е�������Ӧ�Ľ��
������ʵ�飩
��� | ʵ����� | ʵ������ | |||
ʵ��1 |
| �Թܢ���δ�������Ա仯 �Թܢ������� | |||
ʵ��2 | �ֱ�����ڿ�����һ��ʱ�� ������ͼ��ʾ��
| �Թܱ�� | 1min | 10min | 24Сʱ |
�� | �ƺ�ɫ | ��ɫ | ���ɫ | ||
�� | �����Ա仯 | �����Ա仯 | �����Ա仯 | ||
�� | ����Щ��ɫ | dz�� | ��ɫ | ||
ʵ��3 | ���� | ƻ��֭����ɫ | |||
����������ۣ�
��1��ʵ��1��֤��ƻ��֭�к��ж��������ʡ��ڸ�ʵ���Т۵�������_____��
��2��ʵ��2�Ģ���FeSO4��Һ���ʵ���������Ϊ_____%����ʵ���У��Թܢڢ�ʵ��Աȵó��Ľ�����_____����ʵ��2�ó��������_____���������������������
��3��Ϊ��֤����II������ʵ��3Ӧ���еIJ���_____��
����˼�����ۣ�
��4��д��һ�ַ�ֹƻ��֭��ɫ�ķ���_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����5�֣��ס��ҡ������ֹ���������ˮ�е��ܽ��������ͼ��ʾ����ش�

��1��ͼ��P���������
��2�������л����������ң���ò��� �ķ����ᴿ��
��3��ʹ30���ӽ����͵ļ���Һ��ɸ��¶��µı�����Һ���ɲ��õ� һ�ַ�����
��4��ʹ50���ס��ҡ����������ʵı�����Һ���µ�10���������������������������
��5����100g 50����ˮ�м���65g���壬����ȫ���ܽ⣬һ��ʱ������в��ּľ�������������Ϊ��ȫ���ܽ⡱��ԭ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
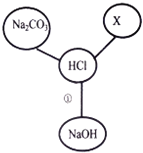
����Ŀ��С��ͬѧ��ѧϰ����Ļ�ѧ����ʱ�����ɳ��������������������Ӧ�Ĺ�ϵ����ͼ��ͼ�С�������ʾ���������������ܷ�����Ӧ����
��1����X�����������ֲ�ͬ���Ļ������X�������� �����ѧʽ��ֻ��һ�ּ��ɣ���
��2��������ͼ��ʾ���ʼ�Ĺ�ϵ��д���ٷ�Ӧ�Ļ�ѧ����ʽ���� ����
��3����X�ǵ���ʱ����д��X��ϡ���ᷴӦ�Ļ�ѧ����ʽ���� ����ֻд��һ�����ɣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ������ֹ������ʵ��ܽ����������ͼ��ʾ����ͼ�ش����⣺
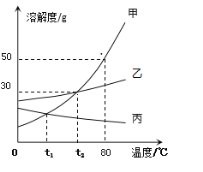
��1��80��ʱ�������ʵ��ܽ����__________��
��2������t1������ʵIJ�������Һ��Ϊ���¶��µı�����Һ���ɲ�ȡ�ķ�����_____������һ�֣���
��3��t2��ʱ���Ѽס��ҡ����������ʵı�����Һ���µ�t1�棬�������������������______��
��4����Ҫ�������ʴ����ı�����Һ��ȫ���ᾧ������Ӧ��ȡ�ķ�����__________��
��5����80��ʱ����150�˼����ʵı�����Һϡ�ͳ���������Ϊ20%����Һ���ˮ____ �ˡ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com