
 µĶÄĘŃĪŹĒŅ»ÖÖ½”æµŹ³ŃĪ£¬ŅŌĘÕĶØÄĘŃĪĪŖ»ł“”Ģķ¼ÓŅ»¶ØĮæĀČ»ÆÄĘ£ØĀČ»ÆÄĘ70%×óÓŅ£¬ĀČ»Æ¼Ų30%×óÓŅ£©£¬ÓŠÖśÓŚČĖĢåÄĘ”¢¼ŲĘ½ŗā£¬½µµĶøßŃŖŃ¹”¢ŠÄŃŖ¹Ü¼²²”µÄ»¼²”·ēĻÕ£®ĮķĶā£¬ÓÉÓŚŹ³ŃĪÖŠµ¼ÖĀĻĢĪ¶µÄŹĒĀČĄė×Ó£¬Ņņ“Ė£¬µĶÄĘŃĪÄܽĻŗĆŹµĻÖ¼õÄĘ²¹¼Ų²»¼õĻĢĪ¶µÄÄæµÄ£®
µĶÄĘŃĪŹĒŅ»ÖÖ½”æµŹ³ŃĪ£¬ŅŌĘÕĶØÄĘŃĪĪŖ»ł“”Ģķ¼ÓŅ»¶ØĮæĀČ»ÆÄĘ£ØĀČ»ÆÄĘ70%×óÓŅ£¬ĀČ»Æ¼Ų30%×óÓŅ£©£¬ÓŠÖśÓŚČĖĢåÄĘ”¢¼ŲĘ½ŗā£¬½µµĶøßŃŖŃ¹”¢ŠÄŃŖ¹Ü¼²²”µÄ»¼²”·ēĻÕ£®ĮķĶā£¬ÓÉÓŚŹ³ŃĪÖŠµ¼ÖĀĻĢĪ¶µÄŹĒĀČĄė×Ó£¬Ņņ“Ė£¬µĶÄĘŃĪÄܽĻŗĆŹµĻÖ¼õÄĘ²¹¼Ų²»¼õĻĢĪ¶µÄÄæµÄ£®·ÖĪö øł¾ŻĢāøÉĢį¹©µÄŠÅĻ¢½ųŠŠ·ÖĪö½ā“š£¬ĻõĖįŅųÄÜÓėĀČ»Æ¼Ų·“Ӧɜ³ÉĀČ»ÆŅų³ĮµķŗĶĻõĖį¼Ų£¬øł¾ŻµĶÄĘŃĪÖŠĀČ»Æ¼ŲµÄŗ¬Įæ¼ĘĖć³öĀČ»Æ¼ŲµÄÖŹĮ棬øł¾Ż·“Ó¦µÄ»Æѧ·½³ĢŹ½¼ĘĖć¼“æÉ£®
½ā“š ½ā£ŗ£Ø1£©Éčѳʷ֊ĀČ»Æ¼ŲÉś³É³ĮµķµÄÖŹĮæĪŖx
ѳʷ֊ĀČ»Æ¼ŲµÄÖŹĮæŹĒ£ŗ2.00g”Į30%=0.6g
KCl+AgNO3ØTAgCl”ż+KNO3
74.5 143.5
0.6g x
$\frac{74.5}{0.6g}=\frac{143.5}{x}$ x”Ö1.16g
·“Ó¦ĖłµĆ³ĮµķµÄÖŹĮæŌ¼ĪŖ1.16g£®
£Ø2£©¶ų“Ėѳʷ֊ɜ³É³ĮµķµÄÖŹĮæĪŖ£ŗ4.51g-3.43g=1.08g£¬¹Ź²»ŗĻøń£»
£Ø3£©ŹµŃéÖŠ“ęŌŚĪó²īµÄæÉÄÜŌŅņŹĒ½ųŠŠµŚŅ»“Ī½ųŠŠ¹żĀĖŹ±£¬ĀĖÖ½ÉĻµÄ³Įµķƻӊȫ²æ±»³ĘĮ棬¹ŹĢī£ŗµŚŅ»“Ī½ųŠŠ¹żĀĖŹ±£¬ĀĖÖ½ÉĻµÄ³Įµķƻӊȫ²æ±»³ĘĮ森
µćĘĄ ±¾Ģāæ¼²éµÄŹĒÓŠ¹Ų»Æѧ·½³ĢŹ½µÄ¼ĘĖć£¬Ķź³É“ĖĢā£¬æÉŅŌŅĄ¾ŻĢāøÉĢį¹©µÄŠÅĻ¢½įŗĻŅŃÓŠµÄ·“Ó¦»Æѧ·½³ĢŹ½½ųŠŠ£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ¼ģŃéCO2ŹĒ·ńŹÕ¼ÆĀś | B£® |  ²āŹŌijČÜŅŗµÄĖį¼ī¶Č | ||
| C£® |  ĮæČ”3mLŅŗĢå | D£® |  ·ÖĄėČÜŅŗÖŠµÄ¹ĢĢ¬ĪļÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
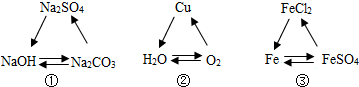
| A£® | ¢Ł¢Ś | B£® | ¢Ł¢Ū | C£® | ¢Ś¢Ū | D£® | ¢Ł¢Ś¢Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŹµŃéÄŚČŻ | ŹµŃé½įĀŪ | |
| A | “ųÓŠ»šŠĒµÄľĢõÖĆÓŚŃõĘųĘæÖŠ£¬Ä¾Ģõø“Č¼ | ŃõĘųÓŠæÉČ¼ŠŌ |
| B | ¶žŃõ»ÆĢ¼ĘųĢåĶØČė×ĻÉ«ŹÆČļŹŌŅŗÖŠ£¬ŹÆČļŹŌŅŗ±äŗģÉ« | ¶žŃõ»ÆĢ¼ÓŠĖįŠŌ |
| C | Ļ”ŃĪĖįµĪČėĒāŃõ»ÆÄĘČÜŅŗÖŠ£¬Ī“¹Ū²ģµ½Ć÷ĻŌĻÖĻó | ¶žÕßƻӊ·¢Éś»Æѧ·“Ó¦ |
| D | ĀČ»ÆøĘČÜŅŗµĪČėijČÜŅŗÖŠ£¬³öĻÖ°×É«³Įµķ | ČÜŅŗÖŠæÉÄÜŗ¬ÓŠCO32- |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 84Ļū¶¾ŅŗŹĒŅ»ÖÖÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄøߊ§ŅŗĢåĻū¶¾¼Į£®Ö÷ŅŖ³É·ÖĪŖ“ĪĀČĖįÄĘ£ØNaClO£©£¬¹ć·ŗÓĆÓŚ±ö¹Ż”¢ĀĆÓĪ”¢Ņ½Ōŗ”¢Ź³Ę·¼Ó¹¤”¢¼ŅĶ„µČµÄĪĄÉśĻū¶¾£®ĒėŌĶĮŠÅĻ¢²¢»Ų“š£ŗ
84Ļū¶¾ŅŗŹĒŅ»ÖÖÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄøߊ§ŅŗĢåĻū¶¾¼Į£®Ö÷ŅŖ³É·ÖĪŖ“ĪĀČĖįÄĘ£ØNaClO£©£¬¹ć·ŗÓĆÓŚ±ö¹Ż”¢ĀĆÓĪ”¢Ņ½Ōŗ”¢Ź³Ę·¼Ó¹¤”¢¼ŅĶ„µČµÄĪĄÉśĻū¶¾£®ĒėŌĶĮŠÅĻ¢²¢»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  µćČ¼¾Ę¾«µĘ | B£® |  ¼ģ²é×°ÖƵÄĘųĆÜŠŌ | ||
| C£® |  ¶Į³öŅŗĢåµÄĢå»ż | D£® |  ŅŗĢåµÄČ”ÓĆ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
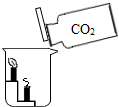 ĶعżŹµŃéĢ½¾ææÉ»ńµĆ½Ļ¶ąµÄ»ÆѧÖŖŹ¶£¬¶ŌČēĶ¼ĖłŹ¾µÄŹµŃé·ÖĪö“ķĪóµÄŹĒ£Ø””””£©
ĶعżŹµŃéĢ½¾ææÉ»ńµĆ½Ļ¶ąµÄ»ÆѧÖŖŹ¶£¬¶ŌČēĶ¼ĖłŹ¾µÄŹµŃé·ÖĪö“ķĪóµÄŹĒ£Ø””””£©| A£® | Į½Ö§ĄÆÖņ×ŌĻĀ¶ųÉĻŅĄ“ĪĻØĆš | B£® | ¶žŃõ»ÆĢ¼²»ÄÜČ¼ÉÕ | ||
| C£® | ¶žŃõ»ÆĢ¼µÄĆܶȱČæÕĘų“ó | D£® | ¶žŃõ»ÆĢ¼Ö§³ÖČ¼ÉÕ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
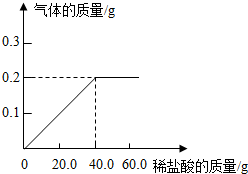 »ĘĶ£ØĶŠæŗĻ½š£©ŹĒÖŲŅŖµÄ½šŹō²ÄĮĻ£¬³£ÓĆĄ“ÖĘŌģ»śŠµĮć¼ž”¢ŅĒ±ķŗĶČÕÓĆĘ·£®ĪŖ²ā¶Øij»ĘĶ²ÄĮĻÖŠŠæµÄŗ¬Į棬»Æѧъ¾æŠ”×é½ųŠŠĮĖŹµŃé£ŗ³ĘČ”15.0g“Ė»ĘĶ²ÄĮĻ£¬ĻņĘäÖŠÖš½„¼ÓČėĻ”ŃĪĖį£¬²ā¶Ø²śÉśĘųĢåµÄÖŹĮæŗĶ¼ÓČėĻ”ŃĪĖįµÄÖŹĮ棬²¢øł¾ŻŹµŃéĒéæö»ęÖĘĮĖ²śÉśĘųĢåÖŹĮæÓė¼ÓČėĻ”ŃĪĖįÖŹĮæµÄ¹ŲĻµĶ¼£®
»ĘĶ£ØĶŠæŗĻ½š£©ŹĒÖŲŅŖµÄ½šŹō²ÄĮĻ£¬³£ÓĆĄ“ÖĘŌģ»śŠµĮć¼ž”¢ŅĒ±ķŗĶČÕÓĆĘ·£®ĪŖ²ā¶Øij»ĘĶ²ÄĮĻÖŠŠæµÄŗ¬Į棬»Æѧъ¾æŠ”×é½ųŠŠĮĖŹµŃé£ŗ³ĘČ”15.0g“Ė»ĘĶ²ÄĮĻ£¬ĻņĘäÖŠÖš½„¼ÓČėĻ”ŃĪĖį£¬²ā¶Ø²śÉśĘųĢåµÄÖŹĮæŗĶ¼ÓČėĻ”ŃĪĖįµÄÖŹĮ棬²¢øł¾ŻŹµŃéĒéæö»ęÖĘĮĖ²śÉśĘųĢåÖŹĮæÓė¼ÓČėĻ”ŃĪĖįÖŹĮæµÄ¹ŲĻµĶ¼£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH4+2O2$\frac{\underline{\;µćČ¼\;}}{\;}$CO2+2H2O | B£® | 3Fe+2CO2$\frac{\underline{\;µćČ¼\;}}{\;}$Fe3O4 | ||
| C£® | NaOH+HClØTNaCl+H2O | D£® | H2CO3ØTCO2”ü+H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com