
【题目】实验室常用氯酸钾和二氧化锰制取氧气,也可用过氧化氢溶液和二氧化锰粉末来制取氧气。请回答下列问题:
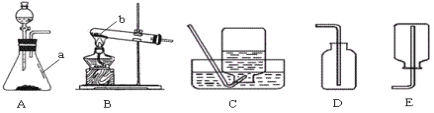
(1)写出图中的仪器名称:a __________, b _______。
(2)向气体发生装置内加入药品前,应该进行的操作是 __________。
(3)用氯酸钾和二氧化锰的混合物制取一瓶干燥的氧气,选择的装置组合是____(填写字母)。写出该反应的化学方程式 __________ 。
(4) 用排水法收集氧气时,依次观察到的现象是____(用字母a、b、c对下图排序);

用排水法收集的氧气中含有氮气的原因可能是_____________(写一点即可)
(5)某学生做铁丝在纯氧中燃烧实验如图所示:
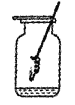
点燃火柴后立即连同铁丝快速深入集气瓶中下部(未接触水),但铁丝未燃烧,针对上述操作,请提出一条改进建议________改进实验后实验成功铁丝在氧气中燃烧的化学方程式是________
(6)若用含过氧化氢0.4mol的双氧水制取氧气,问可制得______mol氧气?(提示:根据化学方程式计算写出计算过程)
【答案】锥形瓶 试管 检查装置的气密性 BD 2KClO3![]() 2KCl+3O2↑ bac 集气瓶没装满水(或没等到有连续均匀气泡冒出就开始收集) 待火柴将要燃尽时连同铁丝由瓶口缓慢伸入集气瓶中下部 3Fe+2O2
2KCl+3O2↑ bac 集气瓶没装满水(或没等到有连续均匀气泡冒出就开始收集) 待火柴将要燃尽时连同铁丝由瓶口缓慢伸入集气瓶中下部 3Fe+2O2![]() Fe3O4 0.2(详见解析)
Fe3O4 0.2(详见解析)
【解析】
(1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据向气体发生装置内加入药品前,应该进行的操作是检查装置的气密性进行分析;
(3)根据实验室用氯酸钾制取氧气的反应物是固体,反应条件是加热,向上排空气法收集的氧气干燥,氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气进行分析;
(4)根据用排水法收集氧气时,先将集气瓶装满水,所以集气瓶中的水逐渐减小,用排水法收集的氧气中含有氮气的原因可能是:集气瓶没装满水(或没等到有连续均匀气泡冒出就开始收集)进行分析;
(5)根据铁丝和氧气在点燃的条件下生成四氧化三铁进行分析;
(6)根据化学方程式和题中的数据进行计算。
(1)通过分析题中所指仪器的名称和作用可知,a是锥形瓶,b是试管;
(2)向气体发生装置内加入药品前,为防止装置漏气,应该进行的操作是检查装置的气密性;
(3)实验室用氯酸钾制取氧气的反应物是固体,反应条件是加热,向上排空气法收集的氧气干燥,所以用氯酸钾和二氧化锰的混合物制取一瓶干燥的氧气,选择的装置组合是BD,氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3![]()
2KCl+3O2↑;
(4)用排水法收集氧气时,先将集气瓶装满水,收集过程中集气瓶中的水逐渐减小,所以依次观察到的现象是bac;用排水法收集的氧气中含有氮气的原因可能是:集气瓶没装满水或没等到有连续均匀气泡冒出就开始收集;
(5)铁丝和氧气在点燃的条件下生成四氧化三铁。铁丝未燃烧,针对上述操作,提出一条改进建议是:待火柴将要燃尽时连同铁丝由瓶口缓慢伸入集气瓶中下部,改进实验后实验成功,铁丝在氧气中燃烧的化学方程式是:3Fe+2O2![]() Fe3O4;
Fe3O4;
(6)设:可以制取氧气物质的量为x

![]() x=0.2mol。
x=0.2mol。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】一种焰火火药中所含的硝酸铜在燃放时产生绿色火焰,发生如下反应:2Cu(NO3)2 ![]() 2CuO + O2↑ + 4X↑。下列有关说法错误的是( )
2CuO + O2↑ + 4X↑。下列有关说法错误的是( )
A. 根据质量守恒定律可知X的化学式为NO2
B. 该反应的基本反应类型为分解反应
C. Cu(NO3)2中铜元素的化合价为+1
D. 产物中CuO属于氧化物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:(提示:稀盐酸与石灰石反应生成二氧化碳和水、氯化钙;与氢氧化钠反应生成水和氯化钠)

(1)提出假设:化学反应中,反应物的总质量与生成物的总质量_____ 。
(2)确定研究方法:分析推理,查阅资料,实验探究。
(3)设计并进行实验:小刚设计的实验装置和选用药品如图A所示,小洁的如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察。
(4)实验结论:通过实验,小刚认为:在化学反应中,生成物的总质量与反应物的总质量不相等,小洁认为:在化学反应中,生成物的总质量与反应物的总质量相等,你认为____的结论正确的,请你谈谈导致另一种结论错误的原因:_____。
(5)结论请从原子的角度,简要分析你认为正确的结论的原因:_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据铁丝在氧气中燃烧的试验,回答下列问题:
①小明做此实验时发现集气瓶底炸裂,请分析一条原因_____________________
②小军发现铁丝没有燃烧,请分析一条原因_________________________
③请写出该反应的化学方程式_________________________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组欲证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较用如图装置进行实验,实验时均以生成25mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
(探究Ⅰ)
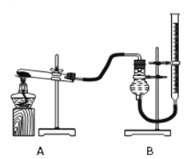
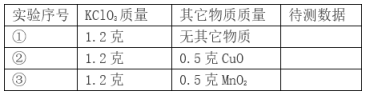
(1)按上图装置仪器组装后,装药品前,首先要做的实验是__________________________。若要证明实验②中球形干燥管内收集的气体是氧气,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上的单孔橡皮塞,把带火星的木条伸入球形干燥管内,木条复燃,证明是氧气;。
(2)实验①和②的目的是______________________________。
(3)为探究CuO在实验②中是否起催化作用,需再做如下实验(无需写出具体操作): a.__________________,b. CuO的化学性质在反应前后有没有改变。
(4)上述实验中的“待测数据”指___________________________________________,若______________说明MnO2比CuO对氯酸钾的催化效果好。
(5)写出氯酸钾被CuO催化分解的符号表达式__________________________。
(探究Ⅱ)研究表明,许多金属氧化物对氯酸钾的分解有催化作用。分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
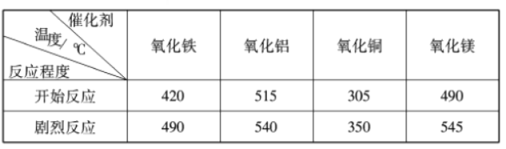
(1)实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用_________(填序号)。
A.氧化铁 B.氧化铝 C.氧化铜 D.氧化镁
(2)实验室加热氯酸钾制氧气时,忘记加入二氧化锰,其结果是___________(填序号)。
A.不能产生氧气 B. 生成氧气的速率慢 C. 产生氧气的总量减少
(探究Ⅲ)
铜的氧化物除了氧化铜(CuO)还有氧化亚铜(Cu2O),请计算:
(1)氧化亚铜的相对分子质量是_____________。
(2)28.8g氧化亚铜中含有__________g铜元素。
(3)当氧化铜与氧化亚铜含铜元素质量相等时,氧化铜与氧化亚铜的质量比是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有A、B、C、D四种物质,其中C为单质,其余均为非金属氧化物,且B为相对分子质量最小的氧化物。它们有如图关系,“![]() ”表示两种物质之间能转化,“ ”表示两种物质之间能相互反应。请回答下列问题:
”表示两种物质之间能转化,“ ”表示两种物质之间能相互反应。请回答下列问题:
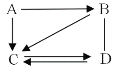
(1)写出B的化学式______,
(2)写出A![]() B的符号表达式___________, B和D反应的符号表达式___________,
B的符号表达式___________, B和D反应的符号表达式___________,
(3)D转化为C的反应,在自然界中可称为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验室制取气体的部分仪器或装置如图所示,请回答下列问题:
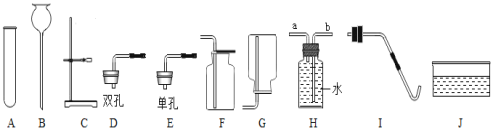
(1)仪器J的名称___________:
(2)若用氯酸钾和二氧化锰制取氧气,必须要增加的一种仪器是________;该反应的符号表达式为______________:。若用装置H收集氧气,氧气应从_____(填“a”或“b”)端通入,若用F装置收集氧气,验满的方法是_______。
(3)某同学用上述(2)中的方法制取氧气,实验过程中试管发生了炸裂,请你帮他分析试管炸裂可能的原因是__________(写一条即可)。
(4)若用过氧化氢溶液和二氧化锰制取并收集干燥的氧气,需要的仪器是______(填字母从A—J中选择),该反应的符号表达式为________。
(5)氨气是一种密度小于空气,极易溶于水的气体,溶于水形成的溶液可以使酚酞试液变红。实验室可用加热氢氧化钙和氯化铵固体混合物的方法制取氨气,实验室可用______方法收集氨气,如果选用如图装置进行制备并验证氨气的性质,当实验开始一段时间之后你会发现酚酞试液变红,且可以看到燃着的蜡烛熄灭。根据信息你认为:玻璃导管没有伸入酚酞试液中的原因是_______;蜡烛熄灭说明氨气_________(填化学性质,任写一条)。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“化学反应条件的控制是实验灵魂”。小林和同学在老师指导下,探究了“影响过氧化氢分解速度的因素”。
(实验)
(1)取两支大试管,分别倒入适量的5%、10%的过氧化氢溶液,再加入等量的二氧化锰,各收集一集气瓶气体,发现浓度大的先收集满。该操作过程中合理的排列顺序____________。(选填序号)
①检验装置的气密性 ②旋紧连有导管的单孔塞
③将水槽中待收集气体的集气瓶注满水 ④有连续稳定气泡再排水集气
⑤向大试管内倒入适量过氧化氢溶液再加入少许二氧化锰粉末
(2)取a 、b两支试管加入等体积5%的过氧化氢溶液,再分别加入少许二氧化锰粉末、氧化铜(CuO)粉末,发现a 中比b中产生气泡多且快。随即用带火星的木条分别悬空伸入试管内,发现a中火星复燃,b中火星仅发亮但不复燃。
( 结论)
根据实验(1)(2)得出影响过氧化氢溶液分解的因素是________________、_____________。
(反思) “红砖粉末是否也可以作过氧化氢分解的催化剂?”
(实验)实验步骤和现象如下:
①小林分别向两支试管中加入等质量等浓度的过氧化氢溶液,向其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体通入水中比较产生气泡的快慢,发现加入红砖粉末的试管中反应较快。
②将反应较快的试管内固体过滤出来,洗涤、烘干。
③用烘干后的固体重复步骤①的实验,现象与步骤①完全相同。
试回答:步骤③的实验目的是___________________________。小林认为通过上述实验已证明红砖粉末可以作过氧化氢分解反应的催化剂,但老师认为小林同学的实验还缺少一个关键步骤,请指出来_______________________________________。
(拓展提高)
小林在实验时,联想到了卖鱼卖虾的商贩用过氧化钙(CaO2)增加水池中的含氧量,于是提出如下猜想.
(猜想)过氧化钙与水反应可制取氧气.
实验装置 | 实验主要过程 |
| ①检查装置气密性. ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体.该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出. |
实验结论:过氧化钙与水反应____________(填“能”或“不能”)用于实验室制取氧气.
(分析与反思)
(1)过氧化钙与水反应虽然没有快速收集到大量氧气,但由此实验现象,小林认为商贩用过氧化钙做增氧剂的主要原因是______________________.
(2)小林希望对此实验进行改进,使该反应加快,请你帮他提出合理化建议_____________.
(计算)该兴趣小组的同学们购得用于增氧的过氧化钙产品(杂质不含钙元素),标签如图所示.试计算:

(1)过氧化钙的相对分子质量为_____________;
(2)过氧化钙中钙元素与氧元素的质量比为____________;
(3)过氧化钙与水反应生成氢氧化钙和氧气,______g过氧化钙与37g氢氧化钙含钙量相当;
(4)该产品(如图)中过氧化钙的质量分数至少为_____________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验是进行科学探究的重要手段,请回答下列问题
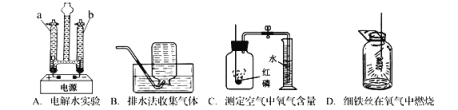
(1)实验A发生反应的化学方程式是__________________________,当电源接通一段时间后,a管与b管中气体的体积比约为__________
(2)实验B集气瓶内装满水的目的是_________________________________
(3)实验C通过______________现象,可得出氧气约占空气体积1/5的结论,若小于1/5,则可能的原因有______________________(答两条原因)
(4)实验D中水的作用是__________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com