
如图是
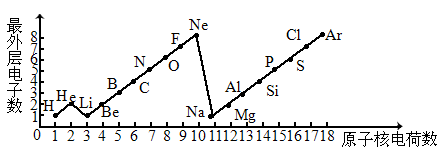
1~18号元素原子最外层电子数与原子核电荷数的关系图,试回答:(1)
一个水分子共有________个原子核,________个质子.(2)
一个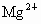 核外共有________个电子;
核外共有________个电子;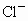 的最外层电子数与________原子的最外层电子数相同.
的最外层电子数与________原子的最外层电子数相同.
(3)
通过对下图的分析,你能发现哪些规律?写出其中的一条.___________________________________________________
.
|
答案: (1)3 10 (2)10 Ne、Ar (3)随着核电荷数的递增,元素原子最外层电子数呈周期性变化(其他合理答案均可).解析:本题考查原子结构、最外层电子数与核电荷数之间的关系,一个水分子中含有两个氢原子和一个氧原子,所以有 3个原子核,1个氢原子有1个质子,共有2个氢原子,1个氧原子有8个质子,故共有10个质子.1个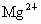 ,是在Mg原子基础上失去了2个电子而形成的,故有12-2=10(个)电子, ,是在Mg原子基础上失去了2个电子而形成的,故有12-2=10(个)电子,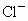 的最外层应有8个电子,与Ar或Ne原子的最外层电子数相同.图像呈现的规律是开放性的,元素的性质由原子最外层电子数决定,最外层电子数出现周期性的变化,则元素的性质也将呈现周期性变化规律.原子中最外层电子数小于4的元素一般为金属元素,易失去电子;最外层电子数大于或等于4的元素一般为非金属元素,易得电子;最外层电子数为8个(氦为2个)的元素为稀有气体元素. 的最外层应有8个电子,与Ar或Ne原子的最外层电子数相同.图像呈现的规律是开放性的,元素的性质由原子最外层电子数决定,最外层电子数出现周期性的变化,则元素的性质也将呈现周期性变化规律.原子中最外层电子数小于4的元素一般为金属元素,易失去电子;最外层电子数大于或等于4的元素一般为非金属元素,易得电子;最外层电子数为8个(氦为2个)的元素为稀有气体元素.
点拨:解答本题时,首先要分析题给信息,确定题目的要求,按要求去发现规律,要多角度的分析、观察,注重对文字信息、表格、数据、图像等信息进行对比分析,发现异同点,将分析上升到普遍性,最后分析得出规律性结论,与所给信息对照,要符合要求,不能违背客观事实. |


科目:初中化学 来源: 题型:
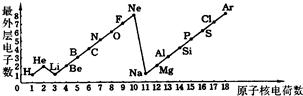 26、如图是1~18号元素原子最外层电子数与原子核电荷数的关系图.试回答:
26、如图是1~18号元素原子最外层电子数与原子核电荷数的关系图.试回答:查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 元素种类 | 举 例 | 原子的最外层电子数 | 得失电子的趋势 | 元素的化学性质 |
| ①金属元素 | Na、Mg、Al | 一般少于4个 一般少于4个 |
失电子 失电子 |
不稳定 不稳定 |
| ②非金属元素 | O、Cl、S、P | 一般多于或等于4个 一般多于或等于4个 |
得电子 得电子 |
不稳定 不稳定 |
| ③稀有气体元素 | He、Ne、Ar | 8个电子(He为2个) 8个电子(He为2个) |
一般不得失电子 一般不得失电子 |
比较稳定 比较稳定 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 图表是整理数据、发现其中规律的一种重要工具,周期表中1---18号元素最外层电子数与原子序数的关系如图所示,试回答:
图表是整理数据、发现其中规律的一种重要工具,周期表中1---18号元素最外层电子数与原子序数的关系如图所示,试回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com