
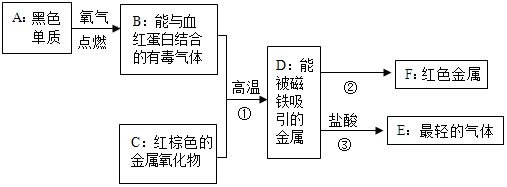
分析 根据B是能与血红蛋白结合的有毒气体,则B为一氧化碳,所以A为碳单质,那么C为氧化铁,D是能被磁铁吸引的金属,初中化学中常见的是金属铁,E是最轻的气体,所以E为氢气,F是常见的紫红色金属,为单质铜,然后将推出的物质进行验证即可.
解答 解:(1)B是能与血红蛋白结合的有毒气体,则B为一氧化碳,所以A为碳单质,那么C为氧化铁,D是能被磁铁吸引的金属,初中化学中常见的是金属铁,E是最轻的气体,所以E为氢气,F是常见的紫红色金属,为单质铜,经过验证,推导正确,所以A是C,E是H2;
(2)反应①是一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
反应②是铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu;
(3)反应③是铁和盐酸反应生成氯化亚铁和氢气,该反应属于置换反应.
故答案为:
(1)C,H2;(2)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,Fe+CuSO4=FeSO4+Cu;(3)置换反应.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:实验探究题
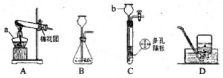 结合图示实验装置,回答下列问题.
结合图示实验装置,回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验编号 | 盐酸的浓度(均取20mL) | 温度/℃ | 收集40mL气体所需时间/s |
| ① | 5% | 30 | 48 |
| ② | 10% | 20 | 41 |
| ③ | 5% | 20 | 69 |
| ④ | 10% | 30 | 32 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
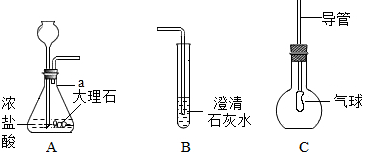 如图为某同学在实验室制取CO2并检验CO2性质的实验装置图.
如图为某同学在实验室制取CO2并检验CO2性质的实验装置图.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 如图为用红磷探究质量守恒定律的实验装置图.请完成下列探究过程:
如图为用红磷探究质量守恒定律的实验装置图.请完成下列探究过程:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 溶液是一类重要的混合物,具有广泛用途.
溶液是一类重要的混合物,具有广泛用途.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com