
分析 (1)铝能被空气中的氧气氧化成氧化铝;
高温条件下,一氧化碳和氧化铁反应生成铁和二氧化碳;
铁能和硫酸铜反应生成硫酸亚铁和铜;
乙炔燃烧生成水和二氧化碳;
(2)根据提供的信息可以判断相关方面的问题;
(3)金属的活动性越强,越不容易被发现和利用;
(4)可燃物燃烧的条件是:与氧气接触,温度达到可燃物的着火点,二者必须同时具备,缺一不可.
解答 解:(1)铝和氧气反应的化学方程式为:4Al+3O2═2Al2O3;
高温条件下一氧化碳能把铁从磁铁矿石(主要成分为Fe304)中还原出来,反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
“曾青(硫酸铜溶液)得铁则化为铜”中包含的化学原理是:Fe+CuSO4═FeSO4+Cu,此反应的基本类型为置换反应;
乙炔完全燃烧的化学方程式为:2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O.
故填:4Al+3O2═2Al2O3;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;Fe+CuSO4═FeSO4+Cu,置换;2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O.
(2)①NH3中氮元素和氢元素的质量比为:14:3;
②将NH3燃烧反应的化学方程式补充完整:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+2N2;
故填:14:3;N2.
(3)金属大规模被使用的先后顺序跟金属的活动性关系最大,金属的活动性越强,越不容易被发现和利用.
故填:C.
(4)在火灾中烟头所起的作用是使可燃物的温度达到着火点.
故填:C.
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.


 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:初中化学 来源: 题型:填空题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 把Mg、Zn、Cu、Ag分别插入同体积、同质量分数的稀盐酸中,比较四种金属的活泼性 | |
| B. | 加热水的方法测定水的组成 | |
| C. | 按溶解、过滤、蒸发的操作顺序分离Na2CO3和BaCO3 | |
| D. | 按方案:NaOH$\stackrel{+稀盐酸}{→}$NaCl$\stackrel{+KNO_{3}}{→}$NaNO3,制取Na |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| OH- | NO3- | Cl- | CO32- | SO42- | |
| H+ | 溶、挥 | 溶、挥 | 溶、挥 | 溶 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 溶 | 不 | 微 |
| Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
| Cu2+ | 不 | 溶 | 溶 | 不 | 溶 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
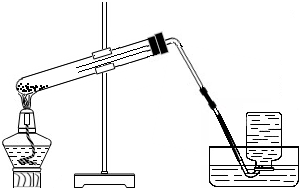 如图是某同学在实验室加热高锰酸钾制取氧气,并用排水法收集的装置图.
如图是某同学在实验室加热高锰酸钾制取氧气,并用排水法收集的装置图.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是一瓶无色无毒的纯净气体
如图是一瓶无色无毒的纯净气体| 猜想 | 检验该气体实验步骤 | 现象及结论 |
| 此气体可能是 氧气 | 将带火星的木条伸入瓶中,木条复燃 | 是氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在纯碱溶液中滴加紫色石蕊试液后溶液变蓝 | |
| B. | 向氯化亚铁溶液中滴加氢氧化钠溶液,生成红褐色沉淀 | |
| C. | 双氧水分解时放出热量 | |
| D. | 聚氯乙烯在空气中灼烧有刺激性气味 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com