
科目:初中化学 来源: 题型:填空题
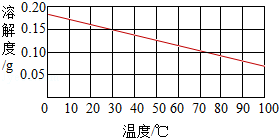 如图是熟石灰的溶解度曲线图,请依据图示信息回答有关问题:
如图是熟石灰的溶解度曲线图,请依据图示信息回答有关问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
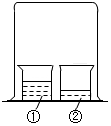 如图实验的烧杯①中液体是浓氨水时烧杯②中的酚酞溶液由无色变为红色;
如图实验的烧杯①中液体是浓氨水时烧杯②中的酚酞溶液由无色变为红色;查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
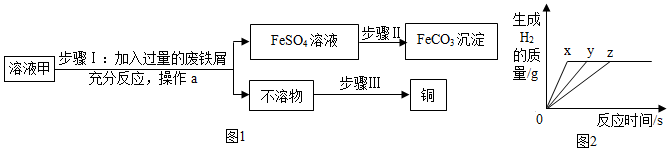
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁 | |
| B. | 氨气遇到湿润的蓝色石蕊试纸,试纸变红 | |
| C. | 浓盐酸敞口放置,瓶口有白烟产生 | |
| D. | 在空气中加热铜丝,表面有黑色固体生成 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
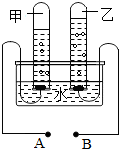 如图是电解水的实验装置图,请根据你所了解的知识填空:
如图是电解水的实验装置图,请根据你所了解的知识填空:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
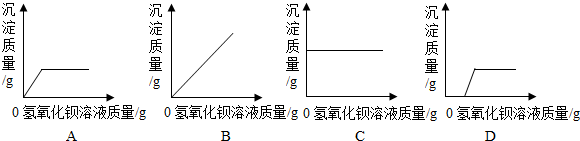
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用纯碱溶液除去水壶中的水垢 | |
| B. | 钢铁制品在干燥的空气中易生锈 | |
| C. | 硫酸铜可用于游泳池水消毒,也可用于自来水消毒 | |
| D. | 用聚乙烯塑料制成的包装袋可包装食品 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com