
同学们从山上采集到一种石灰石(主要成分为碳酸钙),他们取80 g该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化,碳酸钙分解成氧化钙和二氧化碳),测得反应后固体氧化钙的质量与反应时间的关系如下表:
反应时间/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
反应后固体的 质量/g | 80 | 75 | 70 | 66 | 62 | 58 | 58 |
请回答下列问题:
(1)当石灰石完全反应后,生成CO2的质量为_______________。
(2)求该石灰石中含CaCO3的质量分数(写出计算过程)__________。
22 g 62.5%。 【解析】(1)由于固体的质量由80g变为58g,减少了22g,说明生成的气体的质量为22g; (2)由于生成的气体的质量为22g,因此可以根据生成的气体的质量即可求出参与反应的碳酸钙的质量, 【解析】 设样品中含CaCO3的质量为x CaCO3 CaO+CO2↑ 100 44 x 22g x=50g 样品中的质量分数=×1... 金钥匙试卷系列答案
金钥匙试卷系列答案科目:初中化学 来源:四川省成都高新区2018年中考化学模拟测试卷 题型:单选题
下列各组变化中,每一转化在一定条件下均能一步实现的是( )

A. ①② B. ②③ C. ①③ D. ①②③
D 【解析】根据所学知识和题中信息知,①碳不充分燃烧,生成一氧化碳,一氧化碳燃烧生成二氧化碳,二氧化碳与过氧化钠反应生成氧气;②铜加热生成氧化铜,氧化铜与硫酸反应生成硫酸铜,硫酸铜与铁反应生成铜;③硫酸钠与氢氧化钡反应生成硫酸钡白色沉淀和氢氧化钠,氢氧化钠与二氧化碳反应生成碳酸钠,碳酸钠与硫酸反应生成硫酸钠,水和二氧化碳。故选D。查看答案和解析>>
科目:初中化学 来源:江苏省泰兴市2018届九年级二模化学试卷 题型:多选题
研究和学习化学,有许多方法。下列方法中所举例错误的是
选项 | 方法 | 示例 |
A | 实验法 | 用木炭做“测定空气中氧气含量”的实验 |
B | 分类法 | 根据组成物质的元素种类,将纯净物分为单质和化合物 |
C | 归纳法 | 根据稀盐酸、稀硫酸等物质的化学性质,归纳出酸的通性 |
D | 类推法 | 根据金属铝能与稀盐酸反应,推测金属铜也能与稀盐酸反应 |
A. A B. B C. C D. D
AD 【解析】A、测定空气中氧气含量的实验中用红磷,不能用木炭,错误; B、根据纯净物中所含元素的多少将纯净物分为单质和化合物,正确; C、稀盐酸和稀硫酸都可以电离出氢离子,故具有相似的性质,正确; D、金属铜在氢元素的后面,故铜没有氢活泼,故铜不能与酸反应置换氢气,错误。故选AD。查看答案和解析>>
科目:初中化学 来源:四川省安岳县2018届理综适应性训练化学部分试卷 题型:填空题
人类社会的文明进步与金属材料的发展关系密切.
(1)钢铁是应用最普遍的金属材料,容易与空气中的________等物质共同作用而生锈,给人们造成巨大的经济损失。
(2)为了满足对钢铁的需要,我国常采用高炉炼铁,写出高炉炼铁原理的化学方程式_____。
(3)铜锌合金的外观与黄金极为相似,市场上一些不法分子以假乱真,祸害百姓。利用简单的化学知识,将其放入稀盐酸中,观察是否有_______产生即可鉴别其真伪。
(4)某废液中含有少量的硝酸银和硝酸铜,取一定量的废液,加入一定质量的铁粉,充分反应后过滤,得到滤渣和滤液,向滤渣中加入稀盐酸,有气泡产生,则滤渣中一定含有的金属是____。
氧气、水 3CO+Fe2O3 2Fe+3CO2 气泡 银、铜、铁(Ag 、 Cu 、 Fe) 【解析】(1)铁生锈是铁与氧气、水共同作用的结果。(2)高炉炼铁的化学方程式:3CO+Fe2O3 2Fe+3CO2 (3)金属活动性顺序中,氢前的金属能与酸反应产生氢气,铜锌合金中的锌能与酸反应生成氢气,所以可根据是否产生气泡来鉴别真伪。(4)金属活动性顺序中,位于前面的金属能把位于后面的金属从其化...查看答案和解析>>
科目:初中化学 来源:四川省安岳县2018届理综适应性训练化学部分试卷 题型:单选题
下列说法正确的是( )
A. 化学反应前后质量不变的原因是:反应前后分子、原子种类都没改变
B. 酸和碱反应生成盐和水。物质 M 能与酸反应生成盐和水,M 就是碱
C. 鉴别CO和CH4两种无色气体,验纯后点燃分别在火焰上方罩一个冷而干燥的小烧杯
D. 除去CO2中少量CO,可将气体点燃
C 【解析】A. 化学反应前后质量不变的原因是:反应前后原子种类、原子个数、原子质量都没改变,错误;B. 酸和碱反应生成盐和水,物质M能与酸反应生成盐和水,M可能是碱,错误;C. 鉴别CO和CH4两种无色气体,验纯后点燃分别在火焰上方罩一个冷而干燥的小烧杯,烧杯内壁有水雾出现的是甲烷,无水雾出现的是一氧化碳,正确;D. CO2不支持燃烧,CO2中少量的CO燃烧不起来,错误。故选C。 ...查看答案和解析>>
科目:初中化学 来源:山东省2017-2018学年八年级下学期期中化学试卷 题型:实验题
某校化学学习小组设计出如图所示装置,并进行白磷燃烧实验。
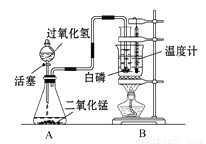
(1)当烧杯内的水受热,温度计显示30℃时,打开活塞,发现盛有水的试管中有气泡均匀逸出,白磷未燃烧,关闭活塞。锥形瓶内反应的化学方程式是_________,白磷未燃烧的原因是_________。
(2)随着水温升高,温度计显示45℃时,再次打开活塞,白磷在水里燃烧。常言道,水火不相容,而本实验中白磷在水里还能够燃烧的原因是__________。
2H2O22H2O+O2↑ 温度未达到白磷的着火点 温度达到着火点,同时又与氧气充分接触 【解析】(1)过氧化氢在二氧化锰的作用下反应能生成水和氧气,化学方程式为:2H2O22H2O+O2↑,白磷的着火点是40℃,白磷未燃烧的原因是温度未达到白磷的着火点; (2)磷在水里还能够燃烧的原因是温度达到着火点,同时又与氧气充分接触。查看答案和解析>>
科目:初中化学 来源:山东省2017-2018学年八年级下学期期中化学试卷 题型:单选题
应用化学知识能有效预防和控制火灾。下面对灭火实例的灭火原理解释不正确的是( )
灭火实例 | 灭火原理 | |
A | 住宅失火时,消防队员用水灭火 | 降低可燃物的着火点 |
B | 酒精在桌上着火时,用湿抹布盖灭 | 隔绝空气或氧气 |
C | 炒菜油锅着火时,用锅盖盖灭 | 隔绝空气或氧气 |
D | 扑灭森林火灾时,设置隔离带 | 可燃物与火源隔离 |
A. A B. B C. C D. D
A 【解析】A、住宅失火时,消防队员用水灭火是将环境温度降到可燃物着火点以下,从而达到灭火的目的,着火点是物质本身固有的属性,不可以降低,错误;B、酒精在桌上着火时,用湿抹布盖灭,是采用隔绝空气或氧气的方法达到灭火的目的,正确;C、炒菜油锅着火时,用锅盖盖熄,是采用隔绝空气或氧气的方法达到灭火的目的,正确; D、扑灭森林火灾时,设置隔离带,是采用隔绝可燃物与火源的方法达到灭火的目的,正确。故...查看答案和解析>>
科目:初中化学 来源:江苏省南京市2018届中考模拟(二)化学试卷 题型:综合题
(经典赏析)我国制碱工业的先驱—侯德榜,发明了将制碱与制氨结合起来的联合制碱法。生产过程是在饱和氨盐水中(NH3和NaCl都达到饱和的溶液)通入 CO2。
(查阅资料)(1)侯氏制碱法中主要反应: Ⅰ.NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl, Ⅱ.2NaHCO3 △ Na2CO3+H2O+CO2↑。
(2) NaHCO3和NH4Cl的溶解度曲线如图所示。

(思考交流)(1)30℃时,NH4Cl饱和溶液中溶质质量分数与NaHCO3饱和溶液中溶质质量分数相比,前者与后者的关系是_______(填字母)。
A.大于 B.小于 C.等于 D.无法确定
(2)反应Ⅰ中生成物NaHCO3和NH4Cl的质量比为_______(不需化简)。
(3)氨盐水吸收CO2后生成NaHCO3和NH4Cl,先结晶析出的物质是NaHCO3,原因是________。
(实验探究)某小组以粗盐和碳酸氢铵(NH4HCO3)为原料,采用以下流程制备纯碱和NH4Cl。
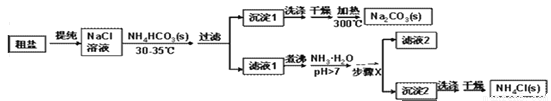
(1)粗盐中除了含有泥沙等不溶性杂质,还含有少量的MgCl2等。若要除去粗盐中的MgCl2,可加入过量的NaOH溶液,过滤,然后向滤液中加入适量盐酸。写出加入盐酸时反应的化学方程式_____________。
(2)过滤时玻璃棒的作用是______________ 。
(3)沉淀1表面常附有NH4+、Cl-等杂质,洗涤时最好选用下列______饱和溶液(填字母)。
A.NaCl B.NH4Cl C. NH4HCO3 D.NaHCO3
(4)步骤X包括的操作有________、冷却结晶和过滤。
(拓展延伸)小华设计下图实验装置测定某纯碱样品(含少量杂质NaCl)中碳酸钠的质量分数:取一定量的样品与足量稀盐酸反应,通过测定生成CO2的体积,计算样品中碳酸钠的质量分数。(已知常温常压下CO2的密度是1.977g/L)
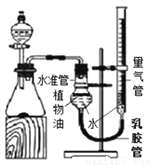
(1)如果样品质量为5.3g,则实验中选用的量气管规格最合适的是_________(填字母)。
A.500mL B.1000 mL C.1500 mL D.2000mL
(2) 反应结束后锥形瓶中有CO2残留,会导致测得的碳酸钠质量分数_________(填字母)。
A.偏大 B.偏小 C.无影响
(3)如果5.3g样品中钠元素的质量分数为42%,实验结束后将锥形瓶中溶液蒸干,则所得固体质量为__________(结果保留1位小数)。
A 84:53.5 反应生成的碳酸氢钠的质量比氯化铵多,且相同温度下碳酸氢钠的溶解度比氯化铵小 NaOH+HCl=NaCl+H2O 引流 D 蒸发浓缩(或蒸发) C C 5.7 g(或5.6 g) 【解析】Ⅱ. (2) 【思考交流】(1) 溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。饱和溶液溶质的质量分数=溶解度÷(溶解度+100g)×100% 。 30℃时,氯化铵的溶...查看答案和解析>>
科目:初中化学 来源:江苏省苏州市2018届九年级上学期第一次月考模拟化学试卷 题型:实验题
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的过程:
(假设)H2O2生成O2的快慢与催化剂种类有关。
(实验方案)常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间。
(进行实验)下图是他们进行实验的装置图,气体发生装置中A仪器的名称是________,此实验中B处宜采用的气体收集方法是_______________。
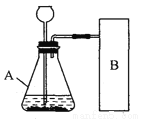
(实验记录)
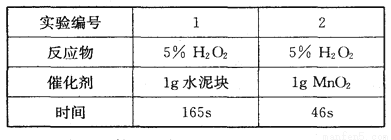
(结论)该探究过程得出的结论是________________________________________。
(反思)H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快。若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的________和_________是否改变。
(实验拓展)H2O2生成O2的快慢还与哪些因素有关?研究性学习小组进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
实验步骤 | 现 象 | 结 论 |
取一支试管加入3~5mL5%的过氧化氢溶液,然后加入少量二氧化锰。 | 缓慢有少量气泡冒出 | _________ |
另取一支试管加入3~5mL15%的过氧化氢溶液,然后加入少量二氧化锰。 | 迅速有大量气泡冒出 |
请你设计:
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
实验步骤 | 现 象 | 结 论 |
____________ | ________ | 温度越高,过氧化氢分解的速率越大 |
____________ | ________ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com