
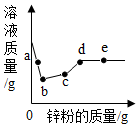
 向一定量硝酸银、硝酸铜和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图.下列说法正确的是( )
向一定量硝酸银、硝酸铜和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图.下列说法正确的是( )| A. | a点时,溶液中溶质为硝酸锌、硝酸铜、硝酸亚铁 | |
| B. | b点时,所得固体只有银 | |
| C. | c点时,溶液中一定有硝酸锌、硝酸亚铁,可能有硝酸铜 | |
| D. | d点和e点所得固体均为银、铜、铁、锌 |
分析 加入锌粉后,锌先与硝酸银反应生成银和硝酸锌,溶液质量减少,锌把硝酸银反应完,再与硝酸铜反应生成铜和硝酸锌,溶液质量增加,溶液质量增加的幅度比较小,锌把硝酸铜反应完,再与硝酸亚铁反应生成铁和硝酸锌,溶液质量增加,增加的幅度增大了,所以b点是锌和硝酸银恰好完全反应,bc段是锌和硝酸铜反应,cd段是锌和硝酸亚铁反应,de段是锌过量.
解答 解:A、b点是锌和硝酸银恰好完全反应,所以a点是锌与硝酸银反应了一部分,所以溶液中溶质为没反应完的硝酸银,生成的硝酸锌和没有反应的硝酸铜、硝酸亚铁,故A错;
B、b点是锌和硝酸银恰好完全反应,锌与硝酸银反应生成银和硝酸锌,所以b点时,所得固体只有银,故B正确;
C、bc段是锌和硝酸铜反应,c点时,锌和硝酸铜恰好完全反应,所以溶液中不存在硝酸铜,故C错;
D、d点是锌和硝酸亚铁恰好完全反应,所以固体中不含有锌,含有银、铜、铁;e点所得固体为银、铜、铁、锌,故D错.
故选B.
点评 解答本题关键是要知道将一种金属加入混合溶液中,金属先与排在最后的盐溶液反应.


科目:初中化学 来源: 题型:实验探究题
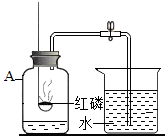 某同学利用如图所示装置来测定空气中氧气的含量.
某同学利用如图所示装置来测定空气中氧气的含量.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物 质 | 杂 质 | 除杂试剂 | 提 纯 方 法 | |
| A | CO | CO2 | O2 | 点燃 |
| B | KCl | MnO2 | 水 | 溶解、过滤、蒸发 |
| C | H2O | NaNO3 | 活性炭 | 吸附、过滤 |
| D | Na2CO3 | Na2SO4 | BaCl2 | 溶解、过滤、洗涤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
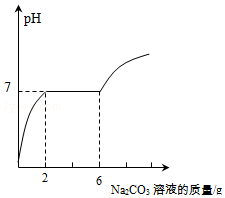 某实验小组的同学用氢氧化钡溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钡溶液加入一定量稀盐酸后,发现忘记了滴加指示剂.因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究:取烧杯中的溶液10g,向其中逐滴滴入溶质质量分数为13.25%的碳酸钠溶液.测得溶液pH与加入的碳酸钠溶液的质量关系如图所示.
某实验小组的同学用氢氧化钡溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钡溶液加入一定量稀盐酸后,发现忘记了滴加指示剂.因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究:取烧杯中的溶液10g,向其中逐滴滴入溶质质量分数为13.25%的碳酸钠溶液.测得溶液pH与加入的碳酸钠溶液的质量关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 为减少白色污染少使用塑料袋 | |
| B. | 高层住房内着火,立即打开所有门窗 | |
| C. | 煤、石油、天然气都属于可再生能源 | |
| D. | 为提高农作物产量,应大量施用化肥 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
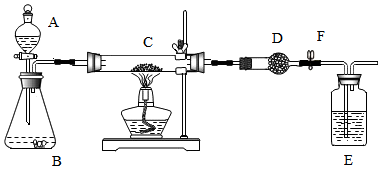
| 实验主要步骤 | 实验现象 | 有关化学方程式 |
| 连接好仪器后,打开止水夹F.检查气密性(观察).在C中加入样品粉末Wg,在D中装入药品后称量为a g | \ | \ |
| 打开A上的活塞,慢慢滴加溶液 | B、E中有气泡 | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ |
| 对C进行加热当C中药品充分反应后,停止加热,通一段时间气体,关闭A的活塞、关F | C中的灰红色粉末变成黑色 | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO |
| 称量D装置的质量为b g | \ | \ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
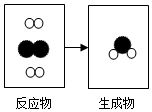 如图是密闭体系中某反应的微观示意图,“
如图是密闭体系中某反应的微观示意图,“ ”和“
”和“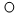 ”分别表示不同原子.请用下列粒子的字母序号回答(1)、(2)两个小题:
”分别表示不同原子.请用下列粒子的字母序号回答(1)、(2)两个小题: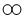 B.
B. C.
C.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com