
【题目】为了测定石灰石样品的纯度( 杂质与稀盐酸不反应)。小组同学设计如下两个方案。
[查阅资料]①纯度=纯物质质量/样品总重量x100%
②无水CaCl2可吸收水蒸气,不与CO2反应
[进行实验]将石灰石研成粉末,每次均取5.0g.稀盐酸每次取浓度、体积均相同且足量。多次实验,求平均值。
方案1 : [实验装置 1]
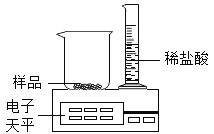
[实验步骤1]
①读取反应前电子天平的示数(m1)
②将稀盐酸全部倒入烧杯中
③待反应停止后,立即读取电子天平的示数(m2)
[实验结果1]纯度平均值为83.8%
方案2: [实验装置 2]
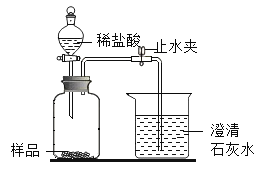
[实验步骤2]
①在气密性良好的装置中装入药品
②称量反应前烧杯和烧杯中液体的质量(m3)
③迅速滴加入过量的稀盐酸后关闭活塞
④反应停止后,立即称量烧杯和其中液体的质量(m4)
[实验结果2]纯度平均值为55.2%
[解释与结论]
(1)方案1中,判断碳酸钙反应完的现象是_____,用实验步骤1中的数据表示出最终生成二氧化碳的质量约是_____。
(2)方案2的装置在装药品前如何检验气密性_____。方案2中烧杯内反应的化学方程式是_____。方案2中测得的样品纯度偏小的原因可能是_____(写一种即可)。
[反思与改进]
为提高测量结果的准确性,对实验1装置按如图进行改进,测得样品纯度的平均值为80.6%。
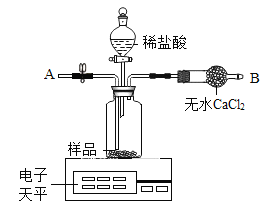
(3)反应前后,两次称量整个装置及药品的总质量。为了测量结果更准确,在第二次称量前,应该进行的操作是_____。
(4)装置中的“无水CaCl2”能提高测量结果的准确性,其原因是_____。
【答案】不再有气泡产生 m1- m2 关闭分液漏斗上的活塞,将右边导管伸入水中,然后两手紧握锥形瓶,若导管口有气泡冒出,说明装置气密性良好 CaCO3+2HCl═CaCl2+H2O+CO2↑ 排出的CO2没有完全被石灰水吸收或者反应容器中CO2有残留 从a口充入空气 可以防止瓶中的水蒸气逸出
【解析】
(1)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳气体,方案1中,判断反应停止的依据是不再有气泡产生;根据质量守恒定律可知,最终生成二氧化碳的质量约是m1- m2;
(2)关闭分液漏斗上的活塞,将右边导管伸入水中,然后两手紧握锥形瓶,若导管口有气泡冒出,说明装置气密性良好;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳气体,反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑;实验2中由于排出的CO2没有完全被石灰水吸收或者反应容器中CO2有残留,故测得的样品纯度偏小;
(3)为保证二氧化碳被全部排出,在第二次称量前,应该进行的操作是从a口充入空气;
(4)装置中的“无水CaCl2”能提高测量结果的准确性,其原因可以防止瓶中的水蒸气逸出。


科目:初中化学 来源: 题型:
【题目】化学的基本特征是研究和创造物质,试从科学家认识物质的视角认识CO2。
(1)分类角度:CO2属于_______(填序号)
A氧化物 B混合物 C单质
(2)微观角度:我国研制的一种新型催化剂可将CO2和H2转化为甲醇(CH3OH)和X。若用“![]() ”表示氢原子、“
”表示氢原子、“![]() ”表示氧原子、“
”表示氧原子、“![]() ”碳原子,该反应的微观示意图如图:
”碳原子,该反应的微观示意图如图:

画出X分子的微观示意图:_______________。
(3)性质角度:三百多年前,人们发现一些洞穴内有一种能使燃烧的木柴熄灭的气体,后来该气体被证实是CO2,据此推测CO2具有的化学性质是:_____________________。
(4)变化角度:如图是某同学整理的物质转化图(已略去反应条件)。在高温条件下,二氧化碳可与某炽热黑色物质反应转变成一氧化碳。写出其反应的化学方程式:________________。

(5)环保角度:全球参与控制CO2的排放量是防止温室效应进一步增强的根本对策。造成大气中CO2含量增加的主要原因是_______(填序号)。
A动植物的呼吸作用
B化石燃料的大量燃烧
C实验室中做实验逸出的CO2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水乃万物之本源,我们生活的地球表面70.8%被水覆盖。请根据所学化学知识填空:
(1)长期饮用硬度过大的水不利于人体健康,生活中常用_______________________________鉴别水是硬水还是软水,在日常生活中常用_______________________________的方法降低水的硬度。
(2)自来水常用氯气杀菌消毒,氯气与水发生反应的化学方程式为:![]() ,其中X的化学式是__________________________________。
,其中X的化学式是__________________________________。
(3)下图所示是水在一些化学实验中的用途,其中分析正确的是_________。
A. 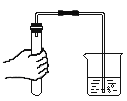 烧杯中的水便于观察是否有气体排出
烧杯中的水便于观察是否有气体排出
B. 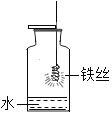 集气瓶中放少量水可以防止集气瓶炸裂
集气瓶中放少量水可以防止集气瓶炸裂
C. 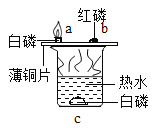 该实验探究燃烧的条件,水只起隔绝氧气的作用。
该实验探究燃烧的条件,水只起隔绝氧气的作用。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小华同学在探究金属与酸反应时,将铝片、锌片打磨后,分别投入盛有等体积、等浓度稀盐酸的试管中,观察到铝与稀盐酸反应较锌与稀盐酸反应快。
(提出问题)金属与盐酸反应快慢,除与金属的种类有关外,还受哪些因素的影响呢?
(猜想与假设)a.可能与盐酸的浓度有关;b.可能与反应时的温度有关;c.你的猜想是________。
实验编号 | 盐酸的浓度(均取20mL) | 温度/℃ | 记录的数据 |
① | 5% | 30 | |
② | 10% | 20 | |
③ | 5% | 20 | |
④ | 10% | 30 |
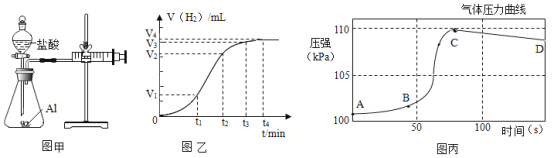
(设计并实验)小明利用图甲所示装置,用不同浓度的盐酸和相同形状的铝片进行如下实验。
(交流讨论)(1)请写出铝与酸反应的化学方程式:____________。
(2)实验前小明先将分液漏斗的活塞关闭,再将注射器活塞往右拉,松手后,观察到注射器活塞回到原处。小明进行该操作的目的是__________。
(分析数据、得出结论)(3)实验中记录的数据可能是:__________;对比实验②③可知_________对金属与酸反应的速率的影响
(4)实验表明,四次实验时反应的速率由快到慢依次为④、②、①、③.根据记录的数据分析,如果盐酸浓度为10%,温度为25℃,则所记录数据应该介于_____________两次实验所记录的数据之间。
(拓展延伸)(5)小明进行铝与稀盐酸反应时,试管外壁发烫,并测得实验过程中生成氢气的体积随时间变化的曲线如图乙所示,根据曲线归纳铝与稀盐酸反应速率的变化规律:___________。
(6)研究小组同学对铝和稀盐酸的反应进行再探究。将橡皮塞连接气体压力传感器,烧瓶中放入图片和稀盐酸,塞紧瓶塞并打开仪器,一段时间后,得到如丙图所示的气体压强与时间的关系曲线图。CD段气体压力逐渐下降的原因是:___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是“白磷燃烧前后质量测定”的实验,下列说法错误的是:

A.细沙能防止锥形瓶炸裂
B.白磷燃烧至熄灭时气球先变大后变小
C.加入白磷的质量和锥形瓶内O2的质量和一定等于生成P2O5的质量
D.装置不漏气最终天平仍平衡
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活中处处有化学,日常生活中许多物质都与化学有关。请回答:
(1)从环保角度考虑,化石燃料、氢气、一氧化碳三类燃料中最理想的是_____。
(2)在汽车电路中,经常用铜作导线,这是利用了铜的_____性。
(3)金属是一种非常重要的资源,在生产、生活中有着广泛的用途。世界上每年钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟_____等物质相互作用的结果。试举一种能减缓钢铁锈蚀的方法_____。工人师傅在焊接钢铁制品时,通常先用稀盐酸清洗制品,原因是(用化学方程式表示)_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小李同学为探究影响金属与酸反应剧烈程度的因素时,进行了如下实验:
步骤 1:调节天平平衡;
步骤 2:将等质量,质量分数都为 10%的稀盐酸倒入烧杯内,分别放在天平的左右两盘;
步骤 3:将等质量的锌粉和铁粉分别放入左,右烧杯内,观察天平的平衡情况;
步骤 4:根据观察到的现象,得出结论。
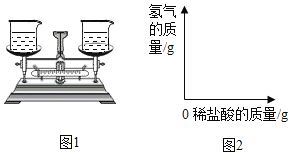
(1)根据实验,我们会观察到,天平开始会向_____倾斜。由此可以得出什么结论_____。
(2)利用天平,我们还可以计算出,金属与酸反应产生的氢气的质量,从而建立相应的坐标关系。如图2是小李做出的等质量的铁和锌与稀盐酸反应的坐标图,请帮他补充完整_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中国在南海海域实现可燃冰试采成功,其主要成分的化学式为CH4nH2O,这标志着我国可燃冰开采技术已居世界前列。
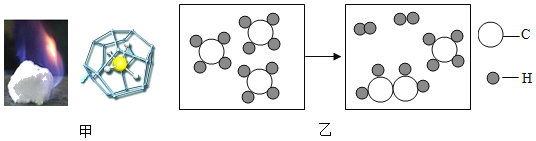
(1)如图甲所示,可燃冰中的水分子形成一种笼状结构,甲烷和少量N2、CO2等分子填入笼内空隙中,由此可知可燃冰属于_____(选填“纯净物”或“混合物”)
(2)若某种可燃冰中CH4与H2O的质量比是1:9,则该可燃冰中n=_____。
(3)图乙表示甲烷在催化剂作用下合成某化工原料的微观示意图。试写出该反应的化学方程式(提示:有机物化学式一般按照C、H顺序来书写):_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是A、B、C三种固体物质的溶解度曲线图示,请根据溶解度曲线图示按要求回答下列问题:
①在t1°C时, 三种物质中溶解能力最强的物质是__________________。 |
|
②若A中含少量的B,提纯A的方法是__________________。 | |
③将t3°C等质量的A、B、C三种物质的饱和溶液降温到t1°C,从溶液里析出较多溶质的是__________________。 | |
④t2°C时,将50克A加入100克水,充分溶解后所得溶液中溶质的质量分数是____________。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com