
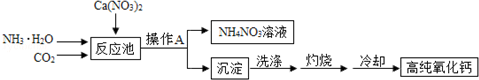
| A. | 反应池中的化学方程式为:CO2+2NH3•H2O+Ca(NO3)2═2NH4NO3+CaCO3↓ | |
| B. | 操作A为蒸发结晶 | |
| C. | 该工艺流程中可以循环使用的物质是CO2 | |
| D. | 冷却需在干燥的环境中进行,否则制得的高纯氧化钙中会混有杂质Ca(OH)2 |
分析 本题是酸碱盐的应用中的物质的制备,由题目的信息可知:冷却需在干燥的环境中进行,否则制得的高纯氧化钙中会混有杂质Ca(OH)2,因为氧化钙与水反应生成氢氧化钙;制备高纯氧化钙的工艺流程中生成的沉淀是CaCO3,因为氨水和二氧化碳和硝酸钙反应生成了碳酸钙白色沉淀和硝酸铵;该工艺流程中可以循环使用的物质是CO2.
解答 解:A、反应池中是氨气、水、二氧化碳和硝酸钙反应生成了硝酸铵和碳酸钙沉淀,其反应的化学方程式为:CO2+2NH3•H2O+Ca(NO3)2═2NH4NO3+CaCO3↓,正确;
B、操作A是过滤,不是蒸发,错误;
C、该工艺流程中可以循环使用的物质是CO2,正确;
D、冷却需在干燥的环境中进行,否则制得的高纯氧化钙中会混有杂质Ca(OH)2,因为氧化钙与水反应生成氢氧化钙,正确;
故选B.
点评 本考点属于实验题中的物质的制备题,综合性比较强,需要掌握酸碱盐的性质,还要掌握相互之间的反应规律和反应的条件.如果物质没有那种性质,就不能造实际上不存在的化学反应.还要注意根据题目给出的信息判断,各有什么注意事项,要把握好.本考点主要出现在实验题和选择题中.


 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将鲜奶发酵制成酸奶 | B. | 在家具生产过程中大量使用甲醛 | ||
| C. | 将燃气热水器安装在浴室内 | D. | 用NaNO2溶液浸泡海鲜,防止变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
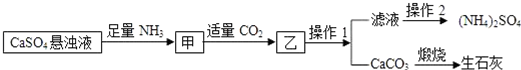
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 安全气囊中选用叠氮化钠的原因可能是NaN3迅速分解产生大量NH3 | |
| B. | 钠可与水反应 | |
| C. | 制备叠氮化钠反应中,主要涉及的化学方程式为:Na+NH3 $\frac{\underline{\;\;△\;\;}}{\;}$NaNH2+H2↑ 2NaNH2+N2O$\frac{\underline{\;\;△\;\;}}{\;}$NaN3+NaOH+NH3↑ | |
| D. | 工业级NaN3中可能含有Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
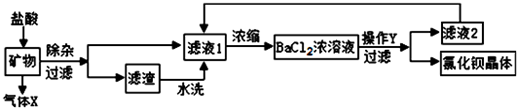
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
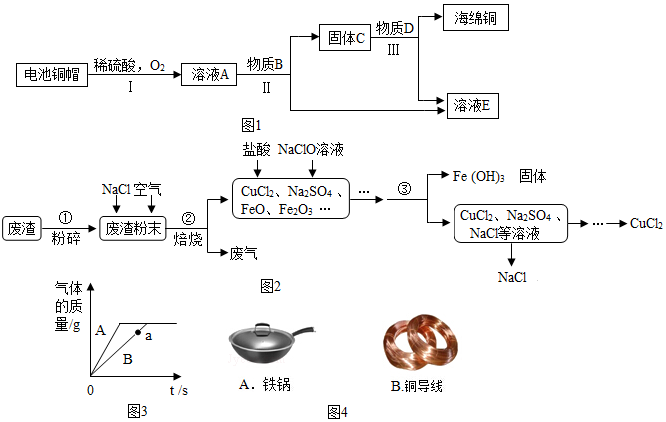
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 试剂 | 稀盐酸 | 食醋 | 蔗糖水 | 蒸馏水 | 肥皂水 | 烧碱溶液 | 石灰水 |
| 颜色 | 红 | 红 | 黄 | 黄 | 绿 | 绿 | 绿 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸使石蕊溶液变红,则能使石蕊溶液变红的物质一定是酸 | |
| B. | 有机化合物一定含有碳元素,则含有碳元素的化合物一定是有机化合物 | |
| C. | 物体吸收热量,内能增加,它的温度不一定升高 | |
| D. | 铁在潮湿的空气中易腐蚀,所以金属在潮湿空气中均易腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com