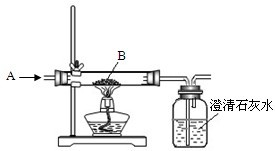
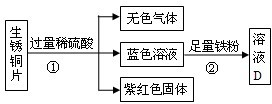
�⣺��1����ҵ�ϣ�������ԭ���ǣ�����һ����̼�Ļ�ԭ�ԣ��������������л�ԭ��������Ӧ�ķ���ʽ�ǣ�Fe
2O
3+3CO

2Fe+3CO
2��
��2������ͭ������Ԫ�غ����⡢̼Ԫ�أ���Ͽ����ijɷֿ�֪����ʽ̼��ͭ[��ѧʽΪCu
2��OH��
2CO
3]��ͭ�������������H
2O ��CO
2 ��ͬ���õĽ����
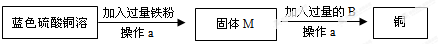
��3��������ɫ��Һ�л���ͭ�Ĺ����У�ͨ������a�ӹ�Һ������еõ��˹��壬���ԣ�����a�������ǹ��ˣ�
�������������ᷴӦ���������ɣ����ԣ�֤��B���������ǣ�����ϡ���ᣬ�����ݲ�����
������ͭ������Ӧ������������������ͭ����Ӧ�ķ���ʽ�ǣ�Fe+CuSO
4=FeSO
4+Cu��
�ʴ�Ϊ����1��Fe
2O
3+3CO

2Fe+3CO
2����2��H
2O��CO
2����3���ٹ��ˣ��ڼ���ϡ���ᣬ�����ݲ�������Fe+CuSO
4=FeSO
4+Cu��
��������1������������ԭ��д����Ӧ�ķ���ʽ��
��2�����������غ㶨�ɼ������ijɷַ�����
��3���ٸ��ݴ���ɫ��Һ�л���ͭ�Ĺ��̣���������a�����ƣ�
�ڸ���������ķ�Ӧ������
�۸�������ͭ�����ķ�Ӧ��д����Ӧ�ķ���ʽ��
������������Ҫ�����˳���������֪ʶ�����������й�����ͭ��֪ʶ���������Ӧ�á����һЩ���⣮

 2Fe+3CO2��
2Fe+3CO2�� 2Fe+3CO2����2��H2O��CO2����3���ٹ��ˣ��ڼ���ϡ���ᣬ�����ݲ�������Fe+CuSO4=FeSO4+Cu��
2Fe+3CO2����2��H2O��CO2����3���ٹ��ˣ��ڼ���ϡ���ᣬ�����ݲ�������Fe+CuSO4=FeSO4+Cu��