
小雨阅读课外资料得知:氯酸钾的分解可用二氧化锰、氧化铜等物质作催化剂。于是,他对影响氯酸钾分解的因素及催化剂的催化效果产生了探究兴趣。
【提出问题】氧化铜是否比二氧化锰催化效果更好?影响氯酸钾分解速率的因素有哪些呢?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列几组实验。
| 序号 | KClO3的质量 | 其他物质的质量 | 温度 | 氧气的体积 | 反应所需时间 |
| ① | 2.0g | | 330℃ | 100mL | T1 |
| ② | 2.0g | CuO 0.5g | 330℃ | 100mL | T2 |
| ③ | 2.0g | MnO2 0.5g | 330℃ | 100mL | T3 |
| ④ | 2.0g | MnO2 g | 380℃ | 100mL | T4 |
(1)> 质量 化学性质
(2)探究氧化铜是否比二氧化锰的催化效果更好
(3)0.5 ;温度越高,反应速率越快;
(4)2KClO3 2KCl+3O2↑
2KCl+3O2↑
解析试题分析:(1) 氧化铜能加快氯酸钾的分解速率,那么收集等体积的氧气所需时间更少,即
t1>t2 ;判断一种物质是否是某反应的催化剂,要看它是否具备催化剂的特征,即“一变二不变”: 能否改变反应的速率;反应前后本身的质量,是否改变;本身的化学性质是否改变。
(2)实验③和实验②分别选用了氧化铜和二氧化锰,催化剂的种类不同,即目的是探究氧化铜是否比二氧化锰的催化效果好。
(3)比较化学反应快慢与温度的关系,应采用控制变量法,即催化剂的质量相同,为0.5g ,t3>t4,则温度低的反应速率更慢,即温度越高,反应速率越快;
(4)实验④是用氯酸钾制取氧气,生成的是氯化钾和氧气,反应的化学方程式为2KClO3 2KCl+3O2↑
2KCl+3O2↑
考点:催化剂、制取氧气的实验原理


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:初中化学 来源: 题型:探究题
某兴趣小组同学对废干电池筒内黑色固体进行探究.
查找资料得知:
①废干电池内含有Mn02、NH4Cl、ZnCl2等;
②NH4Cl具有铵态氮肥的性质;
③向ZnCl2溶液中逐滴滴入稀氨水,先生成Zn(OH)2白色沉淀,然后沉淀溶解,生成可溶性的
[Zn(NH3)4]Cl2.
据此,该兴趣小组同学进行了如下探究:
(1)检验Mn02的存在.兴趣小组同学设计了如图所示的实验:
操作②的名称是 ,该操作中玻璃棒的作用是 .
操作③灼烧黑色滤渣时,会产生一种能使澄清石灰水变浑浊的气体,该气体为 .
操作④的试管中产生的气体能使带火星的木条复燃,该气体为 .
由此得出结论:滤渣中除含有 外,还含有黑色粉末 .
(2)猜想1:滤液中溶质的主要成分为NH4Cl.
操作:取少量滤液加入盛有NaOH固体的试管,并加热.未闻到明显的刺激性气味,但用紫色石蕊试纸放在试管口一段时间,试纸变蓝色.
实验结论:该滤液中含有少量的NH4Cl.
(3)猜想2:滤液中溶质的主要成分为ZnCl2.向盛有少量滤液的试管中逐滴加入 ,观察到 .
实验结论:滤液中溶质的主要成分是ZnCl2.
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
研究盐类物质的性质时,甲、乙、丙三位同学分别向NaHCO3溶液中滴加石灰水,均产生白色沉淀.他们分别设计实验方案,对自己过滤后的滤液中溶质的成分进行如下探究.
【实验准备】
用一定溶质的质量分数的NaHCO3溶液、NaOH溶液和Na2CO3溶液进行如下实验,为设计实验方案提供参考.
| | NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 |
| 加入酚酞溶液 | 溶液变红 | 现象Ⅰ | 溶液变红 |
| 加入CuSO4溶液 | 产生气泡和蓝色沉淀 | 现象Ⅱ | 产生气泡和蓝色沉淀 |
| 加入CaCl2溶液 | 无明显变化 | 无明显变化 | 产生白色沉淀 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
| 实验操作 | 实验现象 | 实验结论 |
| ① ② | ① ② | 滤液中的溶质是Na2CO3和NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
小明发现家中一枚戒指生满了铜绿,他和同学利用这枚戒指展开了研究性学习。
[查阅资料]
①真金在空气中不会生锈,生满铜绿的“金戒指”材质为铜锌合金;
②铜长期露置在潮湿的空气中能生成铜绿,其主要成分是碱式碳酸铜[Cu2(OH)2CO3],
碱式碳酸铜受热易分解生成CuO、H2O和CO2。据上述资料可推知,碱式碳酸铜
由 种元素组成。
[实验探究]
将该枚生满铜绿的戒指加入过量稀盐酸中,有气泡产生,溶液由无色逐渐变为蓝绿色。
(1)小明认为:气体中除了含有CO2外,还可能含有的气体是 。产生该气体的化学反应方程式为 。
(2)小华认为蓝绿色溶液中除含有氯化锌外,还应该含有 、 。他取适量上述蓝绿色溶液,加入光亮的铁片,观察到了现象:① ,② ,从而证实了自己的观点。
(3)小娟取适量新制的FeCl2溶液,加入锌粒,一段时间后,溶液颜色变浅。发生反应的化学方程式为 。结合小华的实验可推知:铁、锌、铜三种金属的活动性由弱到强的顺序是 。
(4)小明想进一步探究“金戒指”中铜元素的质量分数,取一枚同材质的“金戒指”,
称得质量为3.8g。在老师的指导下,将“金戒指”经浓硝酸氧化、碱化等步骤处
理后,最终得到纯净的氧化铜,称得质量仍然为3.8g(实验过程中铜元素损失忽
略不计)。则“金戒指”中铜元素的质量分数是多少?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
化学是以实验为基础的自然科学,通过实验现象的观察和分析得到结论。结合下列实验回答问题。
图A所示实验集气瓶中的现象是:铁丝在氧气中剧烈燃烧,__________,放出大量的热,有黑色固体生成,该反应的符号表达式是_____________。
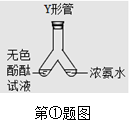
图B所示实验可观察到酚酞溶液由________色变为__________色,该实验中没有涉及的性质是_________(填字母)。
A.氨分子是不断运动的 B.氨分子有一定质量 C.浓氨水具有挥发性
图C所示实验用于测定空气中氧气的含量。红磷在空气中燃烧的符号表达式是______________,关于该实验的下列说法中正确的是__________(填字母)。
A.实验时红磷一定要足量 B.点燃红磷前先用弹簧夹夹紧乳胶管
C.红磷熄灭后立刻打开弹簧夹 D.最终进入瓶中水的体积约为氧气的体积
E. 该实验必须检查装置的气密性
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
在老师的指导下,同学们进行了有趣的化学实验探究:
一、测定空气中氧气含量
图1所示的是小亮同学用红磷在空气中燃烧的测定方法.过程是:
第1步:将集气瓶容积划分为五等份,并做好标记.
第2步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧。
第3步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5.请回答下列问题:

①第2步红磷燃烧时的现象 ,
化学反应表达式: 。
②实验完毕,若进入集气瓶中水的体积不到总容积的1/5,
你认为导致这一结果的原因可能是 。
A、集气瓶底部的水占了一部分体积
B、红磷过少
C、红磷没有燃烧完就急着打开了止水夹
③小博同学对实验进行反思后,提出了改进方法(如图2所示),小博在正式开始实验前,夹紧弹簧夹,将注射器活塞从20mL刻度处推至15mL处,然后松开活塞,观察到活塞返回至20mL刻度处.该操作的主要目的是 ,你认为改进后的优点是 。
二、小余阅读课外资料得知:双氧水分解除了用二氧化锰(MnO2)还可用氧化铜(CuO)等物质作催化剂,于是他对氧化铜产生了探究兴趣。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小余以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验
的因素均忽略)
| 实验序号 | 氯酸钾质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g | |

查看答案和解析>>
科目:初中化学 来源: 题型:探究题
将一张滤纸(组成元素为C、H、O)用FeCl3浓溶液浸润,在酒精灯上烘干后点燃,滤纸变黑、红热,最终转化为黑褐色物质。针对该黑褐色物质,甲同学认为其中含有单质铁;乙同学则认为不含单质铁。为验证各自的猜想,他们进行了如下探究:
(1)甲同学将黑褐色物质放入稀盐酸中,发现有连续的微小气泡产生。如果黑褐色物质中含有单质铁,则反应的化学方程式为 。
(2)乙同学提出疑问:(1)中实验产生的气泡也可能是滤纸碳化后吸附的空气。为此,甲同学又做了(1)中实验的对比实验: ,观察到有微小气泡产生,但很快停止。证明(1)中实验产生的连续的微小气泡是由铁与稀盐酸反应产生的。
(3)通过以上探究,乙同学赞同甲同学的观点,在甲同学的启发下,乙同学提出了另一种证明黑褐色物质中含有单质铁的方法:将黑褐色物质放入硫酸铜溶液中,观察到 现象,说明其中含有单质铁。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
小华和小红对市场上销售的一种袋装的薯片产生了兴趣,因为薯片包装在充满气体的小塑料袋内,袋内的气体充得鼓鼓的,看上去好像一个小“枕头”。他们认为这种充气包装技术主要为了使薯片防腐、防碎。那么,这是什么气体呢?
小华猜想是氮气,小红猜想是二氧化碳。
(1)请你帮助他们设计一个简单的实验方案 ,来判断小红的猜想是否正确,简要写出操作步骤:__________________________________________________________________。
(2)小红的猜想如果正确,现象是____________________________________。
(3)你认为食品充气包装对所充气体的要求是________、____________(至少写2点)
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
只有氧气才能支持燃烧吗?某学习小组对这个问题进行如下探究。
【信息给予】钠是一种银白色的金属,能与空气中的氧气与水蒸气反应。
【提出问题1】除氧气外,是否还有其他物质也能支持燃烧。
【进行实验一】如图,向盛有金属钠(Na)的硬质玻璃管中通入纯净、干燥的CO2,当观察到澄清石灰水中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,钠剧烈燃烧,产生白烟,燃烧结束后玻璃管中有黑色颗粒和白色固体生成。
【得出结论】二氧化碳 ① (“能”或“不能”)支持某些物质燃烧。
【反思评价】点燃酒精灯前,要先向玻璃管中通会二氧化碳,其目的是____②_____。
【提出问题2】黑色颗粒和白色固体是什么?
【猜想与假设】黑色颗粒可能是 ③(用化学式填写)。
【进行实验二】现象:黑色颗粒逐渐减少,澄清石灰水_________④__________。
【得出结论】实验二证明:黑色颗粒的猜想是正确的。
某同学对白色固体的成分做出猜想:(Ⅰ)碳酸钠(Ⅱ)氢氧化钠。
你认为猜想 ⑤ (填序号)一定是错误的,理由是 ⑥ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com