
| A. | KOH和NaOH | B. | NaOH和HCl | C. | Ba(OH)2和H2SO4 | D. | NaOH和HNO3 |
分析 根据复分解反应发生的条件可知,若物质之间相互交换成分不能生成水、气体、沉淀,则能够在溶液中大量共存,据此进行分析判断即可.
解答 解:A、KOH和NaOH在溶液中相互交换成分不能生成沉淀、气体、水,能在溶液中大量共存,故选项正确.
B、NaOH和HCl在溶液中相互交换成分生成氯化钠和水,不能大量共存,故选项错误.
C、Ba(OH)2和H2SO4在溶液中相互交换成分生成硫酸钡沉淀和水,不能大量共存,故选项错误.
D、NaOH和HNO3在溶液中能相互交换成分生成硝酸钠和水,不能大量共存,故选项错误.
故选:A.
点评 本题考查物质的共存问题,判断物质在溶液中能否共存,主要看溶液中的各物质之间能否发生反应生成沉淀、气体、水.


科目:初中化学 来源: 题型:填空题
 20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图1所示的现象.
20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图1所示的现象.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 比较项目 | 实验操作 | 实验现象 | 结论 |
| 二氧化碳 的含量 | 将澄清石灰水分别滴入盛有教室内的空气和操场上的空气的集气瓶中 | 教室内的空气瓶中澄清石灰水变浑浊;操场上的空气瓶中澄清石灰水不变浑浊 | 教室内的空气中二氧化碳含量比操场上的空气中高 |
| 氧气的含量 | 将燃着的蜡烛分别放入盛有教室内的空气和操场上的空气的集气瓶中,盖上玻璃片 | 教室内的空气瓶中蜡烛很快熄灭;操场上的空气瓶中蜡烛过一会熄灭 | 教室内的空气中氧气含量比操场上的空气中低 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 指出图中倾倒液体药剂时的错误并改正:
指出图中倾倒液体药剂时的错误并改正:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
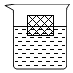 将一块塑料板放入50℃的硝酸钾饱和溶液中,塑料板漂浮于液面上(如图).若将溶液降温到20℃时,可观察到的现象是塑料板下沉,有晶体析出若要看到塑料板上浮,应采用的方法是加入氯化钠等其它物质.
将一块塑料板放入50℃的硝酸钾饱和溶液中,塑料板漂浮于液面上(如图).若将溶液降温到20℃时,可观察到的现象是塑料板下沉,有晶体析出若要看到塑料板上浮,应采用的方法是加入氯化钠等其它物质.查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com