




 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
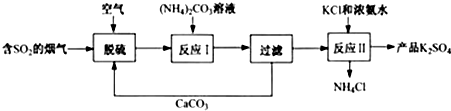
某热电厂用脱硫得到的石膏(CaSO4•2H2O)生产K2SO4肥料的流程如下.

请回答下列问 题:
题:
(1)石膏中S的化合价是 .脱硫过程的化学方程式为2CaCO3+2SO2+O2+4H2O=2CaSO4•2H2O+2 .
(2)石膏与饱和(NH4)2CO3溶液相混合,发生反应Ⅰ时需不断搅拌,其目的是 .
(3)实验室完成过滤操作所需要的仪器有铁架台、玻璃棒以及 (填字母序号),玻璃棒的作用是 .

(4)(NH4)2SO4与KCl溶液需在浓氨水中发生反应Ⅱ,析出K2SO4晶体.此反应的基本类型是 ,浓氨水的作用是 ,反应Ⅱ需在密闭容器中进行的原因是 .
(5)该工艺可以循环利用的物质有 (写一种),副产品NH4Cl与NaOH溶液混合微热,产生的气体能使湿润的红色石蕊试纸变 色.
查看答案和解析>>
科目:初中化学 来源:2013年初中毕业升学考试(江苏扬州卷)化学(解析版) 题型:简答题
某热电厂用脱硫得到的石膏(CaSO4•2H2O)生产K2SO4肥料的流程如下.
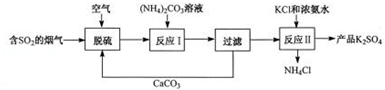
请回答下列问题:
(1)石膏中S的化合价是 .脱硫过程的化学方程式为2CaCO3+2SO2+O2+4H2O=2CaSO4•2H2O+2 .
(2)石膏与饱和(NH4)2CO3溶液相混合,发生反应Ⅰ时需不断搅拌,其目的是 .
(3)实验室完成过滤操作所需要的仪器有铁架台、玻璃棒以及 (填字母序号),玻璃棒的作用是 .
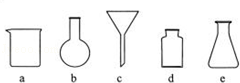
(4)(NH4)2SO4与KCl溶液需在浓氨水中发生反应Ⅱ,析出K2SO4晶体.此反应的基本类型是 ,浓氨水的作用是 ,反应Ⅱ需在密闭容器中进行的原因是 .
(5)该工艺可以循环利用的物质有 (写一种),副产品NH4Cl与NaOH溶液混合微热,产生的气体能使湿润的红色石蕊试纸变 色.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com