
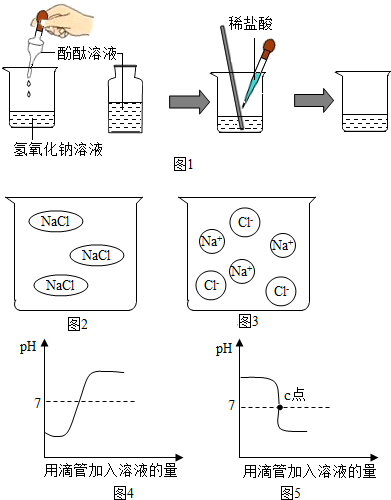
 ��ͼ��գ�
��ͼ��գ����� ��1�������������������ᷴӦ�����Ȼ��ƺ�ˮ���з�����
��2����������������������кͷ�Ӧ�����Լ�����ʽ�������Һ�ĵ����Է������
��3����������������Һ�Լ��ԣ�pH����7��ϡ���������ԣ�pHС��7���з�����
��4�������������ƺ����ᷴӦ�ķ���ʽ���г�������ϵ������⣮
��� �⣺��1��ϡ����������������Һ��Ӧ�����Ȼ��ƺ�ˮ����ѧ����ʽΪ��HCl+NaOH=NaCl+H2O��
��2������������ʹ��̪���ɫ��ϡ����������������Һ��Ӧ�����Ȼ��ƺ�ˮ����ǡ����ȫ��Ӧʱ����Һ�����ԣ��ɺ�ɫ��Ϊ��ɫ��
�Ȼ�������ˮ�����������Ӻ������ӣ���ͼ3���Դ�����ʱ����Һ�������е����ӣ�������Һ�����ԭ���Ǵ��������ƶ������ӣ����Կ�������Һ�ĵ�����ʵ��֤���Ȼ�����Һ���Ƿ������ӣ�
��3������������Һ�Լ��ԣ�pH����7��ϡ���������ԣ�pHС��7��ϡ����������������Һ��Ӧ�����Ȼ��ƺ�ˮ��������������ļ�����Һ�ɼ��Ե������ٵ����ԣ�pH���ɴ���7������7�ٵ�С��7������Ϊͼ5��ʾ��
��4����Ҫ����������Һ������Ϊx��
NaOH+HCl=NaCl+H2O
40 36.5
20%��x 36.5%��40g
$\frac{40}{20%��x}$=$\frac{36.5}{36.5%��40g}$
x=80g
�ʴ�Ϊ����1��HCl+NaOH=NaCl+H2O��
��2����Һ�ɺ�ɫ��Ϊ��ɫ��ͼ3����Һ�ĵ�����ʵ�飻
��3��ͼ5��
��4��80g��
���� ������Ҫ�����˸���ͼ����кͷ�Ӧ����ȷ���жϺ����⣬�ѶȲ����ۺ���ǿ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����к���ˮ | |
| B�� | ����ȼ��ʱ������ˮ | |
| C�� | �����ǿ����е�ˮ��������֤��ʲô | |
| D�� | ���ܶ���ȷ������Ҫ�н�һ����ʵ��֤�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ᡢ��ʯ�ҡ����� | B�� | ���ᡢ����Ȼ��� | ||
| C�� | ̼�ᡢ�ƾ����մ� | D�� | ���ᡢ��ˮ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
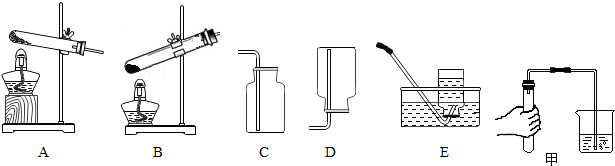
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe | B�� | Al | C�� | Zn | D�� | Ag |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
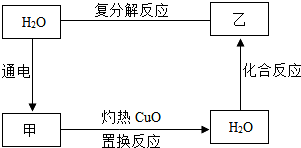 ˮ����Ȼ����Ϊ��Ҫ�����ʣ���ͼ��ʾˮ�������������ʼ��һ��ѭ��ת����ϵ�����ַ�Ӧ���������δ���������ɼ��ǵ��ʣ�������Ϊ�����Է�������Ϊ74��
ˮ����Ȼ����Ϊ��Ҫ�����ʣ���ͼ��ʾˮ�������������ʼ��һ��ѭ��ת����ϵ�����ַ�Ӧ���������δ���������ɼ��ǵ��ʣ�������Ϊ�����Է�������Ϊ74���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����һ�ֻ����� | |
| B�� | ���ط�����̼����ԭ�Ӹ�����Ϊ1��4 | |
| C�� | ������̼����������������Ԫ����� | |
| D�� | �����е�Ԫ�ص���������=$\frac{14}{60}$��100%=23.3% |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com