
【题目】元素周期表中,同周期元素的结构和性质呈现一定的规律性变化。下表列出的是第三周期元素的原子半径及主要化合价(部分信息未列出)。下列有关说法不正确的是( )
元素 | Na | Mg | ① | Si | P | ② | Cl |
原子的最外层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
原子半径(10-10m) | 1.86 | 1.60 | 1.43 | ③ | 1.10 | 10.2 | 0.994 |
最高正价最低负价 | +1 | +2 | ④ | +4 -4 | +5 -3 | ⑤ | +7-1 |
A.⑤处的最高正价是+6,最低负价是-2
B.元素①的原子序数是 13,①和②形成的化合物的化学式为 AlS
C.第三周期元素(Na→Cl)的最高正价数等于其原子的最外层电子数
D.③处的数值介于 1.10~1.43 之间
【答案】B
【解析】
根据表格中各项的变化规律:第三周期元素从左至右依次为 Na、Mg、Al、Si、P、S、Cl,原子的最外层电子数依次增大,由1逐渐增加到7;原子半径依次减小;最高正价从+1到+7,最低负价从-4到-1;则有:
A、化合价从+1至+7依次增大,从Si开始有变价,负价逐渐减小,故④为+3价,⑤最高正价是+6,最低负价是-2,A选项说法正确,不符合题意;
B、第三周期元素从左至右依次为Na、Mg、Al、Si、P、S、Cl,所以①是 Al,原子序数是13,②是S,铝显+3价,硫显-2价,二者形成的化合物的化学式为![]() ,B选项说法不正确,符合题意;
,B选项说法不正确,符合题意;
C、第三周期元素(Na→Cl)的最高正价数等于其原子的最外层电子数,C选项说法正确,不符合题意;
D、由表中信息可知元素原子的半径逐渐减小,③处的数值介于1.10-1.43之间,D选项说法正确,不符合题意。故选B。


科目:初中化学 来源: 题型:
【题目】化学就在我们身边,它与我们的生活息息相关。
(1)“健康饮食、均衡营养”是青少年健康成长的重要保证。下列物质中富含蛋白质的有________(填字母)。
A 米饭和馒头 B 大豆油和花生油 C 牛肉和鸡蛋 D 蔬菜和水果
(2)“食品安全”是一个永恒的话题。你认为下列认识科学的是________(填字母)。
A 任何食品都不可以使用食品添加剂
B 霉变的大米、花生,即使经过蒸煮也不能食用
C 含钙、锌的奶粉有利于补充人体所需的常量元素
D 用工业用盐亚硝酸钠代替食盐来腌渍食品
(3)生活中可用__________鉴别硬水和软水。
(4)加入洗涤剂的水能除去衣服上的油污,是利用了洗涤剂的________作用。
(5)尿素是一种常用的化肥,工业上生产尿素反应的微观示意图如图:
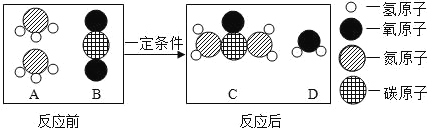
该反应中两种反应物A和B的质量比为_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有FeCO3和CuO的混合物31.2g,进行如下实验,把混合物全部加入到100g适量的硫酸溶液中,恰好完全反应溶解,然后滴加适量的质量分数为16%的氢氧化钠溶液,直到恰好不再有沉淀生成,共用去150g 氢氧化钠溶液,混合物中FeCO3的质量分数为( )
A.30%B.74.4%C.70%D.25.6%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们在学完酸的化学性质后,做了如下实验:
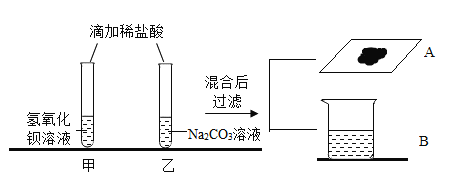
[观察与讨论1]乙试管中观察到_____现象,小组的同学们将实验后溶液混合起来对废液进行处理,混合过程中产生气泡,于是小组同学得出反应后甲试管中的溶质是_____,充分反应后过滤,得到滤液B和滤渣A,向滤渣中加稀硝酸,发现固体表面产生气泡,同学们接着对滤液B中的成分进行探究。
[提出问题1]滤液B中的含有哪些离子?
[猜想与假设]小欣同学猜想:Na+、Cl-
小研同学猜想:Na+、Cl-、SO42-
小洋同学猜想:Na+、Cl-、Ba2+、H+
你的猜想_____(一种即可)
[实验与探究]小研同学认为不需要证明就可得出_____的结论是错误的。
小研同学为证明自己猜想正确,取滤液少量加入足量的氯化钡溶液,发现溶液中产生白色沉淀,继续加入足量稀盐酸,一段时间后观察,固体不消失,则证明自己结论正确。请你对她的结论进行评价_____。
为了进一步证明滤液中离子成分,小群同学取滤液少量加入_____,根据产生的现象即可得出滤液中的离子成分。
[归纳总结]通过以上实验我们能够总结出,在研究反应后溶液中离子成分时,首先应该根据实验现象判断出_____的离子是一定不存在的。在探究过程中,加入试剂后,对物质在_____的现象,进行系统地、细致地观察和描述,得出可靠的结论。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】汽车尾气中含有许多有害气体,使用催化转换器可减少有害气体的排放,其中某一反应过程的微观变化如图所示。
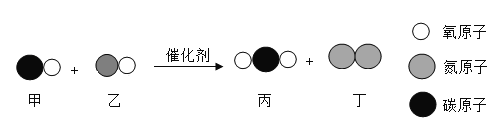
(1)请标出丁中所含元素的化合价________;
(2)甲、乙、丙、丁四种气体中密度最大的是_________(填序号),保持丙物质化学性质最小的粒子是________(填名称);
(3)参加反应的甲与乙的质量比是_________;
(4)尝试写出该转化过程的化学方程式_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸钙转化学 K2SO4和 CaCl2.6H2O 的工艺流程如下:
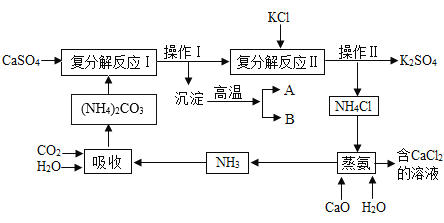

(1)吸收过程中发生了化合反应,化学方程式为____。
(2)操作Ⅰ的名称为_,沉淀的主要物质为____(填化学式)。
(3)复分解反应Ⅱ的化学反应方程为:_______。操作Ⅱ包含的操作是__。
(4)蒸氨过程中涉及的化应类型为_____(填编号)
A 复分解反应
B 化合反应
C 分解反应
D 置换反应
(5)操作Ⅲ包含一系列操作:蒸发浓缩、_____、过滤、洗涤、干燥。
(6)可循环利用的物质除了 NH3外,还有____(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是在分子、原子层次上研究物质的科学。

(1)构成物质的粒子有分子、原子和____________。
(2)图为三种元素的原子结构示意图。氧原子在化学反应中容易____________电子(填“得到”或“失去”)。
(3)二氧化硫和二氧化碳都能与氢氧化钠溶液反应生成盐和水。将二氧化硫气体通入氢氧化钠溶液中生成亚硫酸钠和水,写出该反应的化学方程式______________。
(4)硒元素与氧、硫元素的化学性质相似,原因是它们原子的______________相同。
(5)硒元素能增强人体免疫力,延缓衰老,山药等食物中富含硒元素。硒(Se)在氧气中燃烧生成二氧化硒。写出硒在氧气中燃烧反应的化学方程式_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】近年来,我国航空、航天、高铁等得到长足发展,跻身世界前列。大飞机C919试飞成功,标志着我国的航空强国又迈出了一大步。大飞机使用的化学材料如图。请回答:
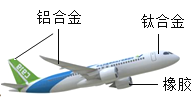
(1)橡胶属于____(填“金属”或“合成”)材料。
(2)如图是钛原子结构示意图,则x=_____;钛元素在化学反应中容易___(填“得到”或“失去”)电子。
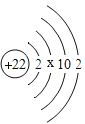
(3)铁比铝的强度大,但制造飞机用铝合金而不用铁合金,主要原因是铝比铁的密度小且抗腐蚀性能强。铝具有很好的抗腐蚀性的原因是____(用化学方程式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质在反应前后的质量关系如图所示下列有关说法不正确的是( )
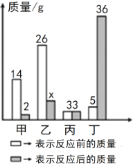
A. 参加反应的甲和乙质量比为14﹕26
B. 丙可能是该反应的催化剂
C. 丁一定是生成物
D. x的值是7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com