
ЎѕМвДїЎїКЄ·ЁТ±Ні§ЕЕ·ЕµД·ПЛ®ЦРє¬УРБтЛбєНБтЛбНБЅЦЦОЫИѕОпЈ¬ОЄІв¶ЁёГ·ПЛ®ЦРёчОЫИѕОпµДє¬БїЈ¬»·±ЈРЎЧйµДН¬С§ЅшРРБЛТФПВКµСйЈ®ИЎ·ПЛ®500gЈ¬ПтЖдЦРјУИлИЬЦКЦКБї·ЦКэОЄ20%µДЗвСх»ЇДЖИЬТєЈ®ІвµГіБµнЦКБїУлЛщјУИлµДЗвСх»ЇДЖИЬТєµДЦКБї№ШПµИзНјЈ®ёщѕЭЛщµГКэѕЭјЖЛгЈє 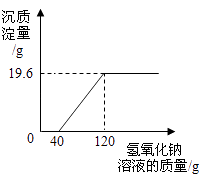
ЈЁ1Ј©500g·ПЛ®ЦРјУИлЗвСх»ЇДЖИЬТєід·Ц·ґУ¦єуЈ¬µГµЅіБµнµДОпЦКµДБїКЗmolЈ®
ЈЁ2Ј©ёГ·ПЛ®ЦРБтЛбНµДИЬЦКЦКБї·ЦКэЈ®ЈЁРґіцјЖЛг№эіМЈ©
ЈЁ3Ј©ёГ·ПЛ®ЦРБтЛбµДОпЦКµДБїКЗ Ј®
Ўѕґр°ёЎї
ЈЁ1Ј©0.2
ЈЁ2Ј©ЅвЈєЙи·ПЛ®ЦРБтЛбНµДОпЦКµДБїОЄxЈ¬ПыєДµДЗвСх»ЇДЖµДОпЦКµДБїОЄyЈ®
CuSO4+2NaOH= | CuЈЁOHЈ©2Ўэ+Na2SO4 |
1 | 1 |
x | 0.2mol |
![]() =
= ![]()
x=0.2molЈ»
ёГ·ПЛ®ЦРБтЛбНµДИЬЦКЦКБї·ЦКэОЄ ![]() ЎБ100%=6.4%
ЎБ100%=6.4%
ґрЈєёГ·ПЛ®ЦРБтЛбНµДИЬЦКЦКБї·ЦКэОЄ6.4%
ЈЁ3Ј©0.1mol
ЎѕЅвОцЎїЅвЈєўЩµГµЅЗвСх»ЇНіБµнµДОпЦКµДБїОЄЈє ![]() =0.2molЈ»ўЫУлБтЛб·ґУ¦µДЗвСх»ЇДЖµДЦКБїОЄ40gЎБ20%=8g УлБтЛб·ґУ¦µДЗвСх»ЇДЖµДОпЦКµДБїОЄЈє
=0.2molЈ»ўЫУлБтЛб·ґУ¦µДЗвСх»ЇДЖµДЦКБїОЄ40gЎБ20%=8g УлБтЛб·ґУ¦µДЗвСх»ЇДЖµДОпЦКµДБїОЄЈє ![]() =0.2mol
=0.2mol
ЙиёГ·ПЛ®ЦРБтЛбµДОпЦКµДБїКЗy
H2SO4+ | 2NaOH=Na2SO4+2H2O |
1 | 2 |
y | 0.2mol |
![]() =
= ![]()
y=0.1molґрЈєўЩ0.2Ј»ўЪ6.4%ўЫ0.1mol
Ўѕїјµгѕ«ОцЎїАыУГёщѕЭ»ЇС§·ґУ¦·ЅіМКЅµДјЖЛг¶ФМвДїЅшРРЕР¶ПјґїЙµГµЅґр°ёЈ¬РиТЄКмЦЄёчОпЦКјдЦКБї±И=ПµКэЎБПа¶Ф·ЦЧУЦКБїЦ®±ИЈ®


 Мб·Ц°Щ·Ц°ЩјмІвѕнПµБРґр°ё
Мб·Ц°Щ·Ц°ЩјмІвѕнПµБРґр°ё
| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєіхЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїЗш·ЦУІЛ®УлИнЛ®їЙУГЈЁ Ј©
A.ХбМЗЛ®
B.·КФнЛ®
C.КіСОЛ®
D.КіґЧ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєіхЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї¶ФИзНјКµСйµД·ЦОцЛµГчІ»ХэИ·µДКЗЈЁ Ј© 
A.ёГКµСйЛµГчТ»Сх»ЇМјѕЯУР»№ФРФ
B.ёГКµСйЛµГчЙъіЙОп¶юСх»ЇМјµДГЬ¶И±ИїХЖшґу
C.ёГКµСйЛµГчТ»Сх»ЇМјєНСх»ЇНµД·ґУ¦РиТЄјУИИ
D.ёГКµСйїЙТФ·АЦ№УР¶ѕµДТ»Сх»ЇМјЖшМе¶ФїХЖшµДОЫИѕЈ¬Н¬К±УЦїЙТФід·ЦАыУГДЬФґ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєіхЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї»ЇС§їЖјјРЎЧйН¬С§ДЈД⹤і§їБ»Ї·ЁЙъІъЙХјоµДКѕТвНјИзНјЈє 
Зл»ШґрПВБРОКМвЈ®
ўЩРґіцмСЙХКЇ»ТКЇµД»ЇС§·ЅіМКЅЈ»ІЩЧч2µДГыіЖКЗ Ј®
ўЪИф·ґУ¦ЖчЦРґїјоИ«Ії·ґУ¦Ј¬µ«Ѕбѕ§µГµЅµД№ММеЙХјоЦР»№є¬УРЙЩБїµДФУЦКЈ¬ФТтКЗ Ј¬ јмСйёГФУЦКСЎУГµДКФјБКЗ Ј¬ јмСйК±№ЫІмµЅ Ј¬ ЛµГчЅбѕ§µГµЅµД№ММеЙХјоИ·Кµє¬УРЙЩБїФУЦКЈ¬ёГ·ґУ¦µД»ЇС§·ЅіМКЅОЄ Ј®
ўЫВЛТєCїЙјУИл·ґУ¦ИЭЖчС»·ФЩАыУГЈ¬ДїµДКЗ Ј®
ўЬИфН¶Ил·ґУ¦ИЭЖчЦРµДґїјоОЄnmolЈ¬ФтОЄБЛИ·±ЈґїјоИ«ІїЧЄ»ЇОЄЙХјоЈ¬Н¶ИлЙъКЇ»ТµДОпЦКµДБїИЎЦµ·¶О§КЗ Ј®
Ійїґґр°ёєНЅвОц>>
їЖДїЈєіхЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїПВБРОпЦКЦРЈ¬ДїЗ°І»јЖИлїХЖшОЫИѕЦёКэµДОпЦККЗЈЁ Ј©
A.Т»Сх»ЇМј
B.¶юСх»ЇМј
C.іфСх
D.їЙОьИлїЕБЈОп
Ійїґґр°ёєНЅвОц>>
їЖДїЈєіхЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїРЎГчУГБ№їЄЛ®СшУгЈ¬І»ѕГУг¶щѕНЛАБЛЈ®ПВБРЅвКНєПАнµДКЗЈЁ Ј©
A.Б№їЄЛ®ЦРјёєхІ»є¬Л®·ЦЧУ
B.Б№їЄЛ®ЦРјёєхІ»є¬Сх·ЦЧУ
C.Б№їЄЛ®ЦРјёєхІ»є¬СхФЧУ
D.Б№їЄЛ®ЦРјёєхІ»є¬СхФЄЛШ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєіхЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїПВБРОпЦКµДУГНѕЦРЈ¬ЦчТЄУ¦УГЖд»ЇС§РФЦКµДКЗЈЁ Ј©
A.УГМъВБЦЖЧчТыѕЯ
B.УГёЙ±щЅшРРИЛ№¤ЅµУк
C.УГѕЖѕ«ЧчИјБП
D.УГНЧчµјПЯ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєіхЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїУРТ»ЦЦОпЦКµД»ЇС§КЅОЄNa2SiO3 Ј¬ ЖдЦРSiµД»ЇєПјЫОЄЈЁ Ј©
A.+1
B.+2
C.+3
D.+4
Ійїґґр°ёєНЅвОц>>
їЖДїЈєіхЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїМоїХ
ЈЁ1Ј©ФЄЛШЦЬЖЪ±нЦР9єЕФЄЛШКфУЪЈЁМоЎ°ЅрКфЎ±»тЎ°·ЗЅрКфЎ±Ј©ФЄЛШЈ¬ФЪ»ЇС§·ґУ¦ЦРТЧЈЁМоЎ°К§ИҐЎ±»тЎ°µГµЅЎ±Ј©µзЧУЈ¬РОіЙЈЁМо»ЇС§·ыєЕЈ©Ј®
ЈЁ2Ј©Ул16єЕФЄЛШФЧУѕЯУРПаЛЖ»ЇС§РФЦКµДФЄЛШКЗ Ј® ЈЁМоФЄЛШ·ыєЕЈ©
Ійїґґр°ёєНЅвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com