
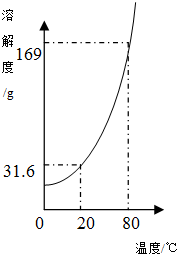
 请根据如图的硝酸钾溶解度曲线,回答下列问题:
请根据如图的硝酸钾溶解度曲线,回答下列问题:科目:初中化学 来源: 题型:
 (2007?哈尔滨)如图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题:
(2007?哈尔滨)如图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:
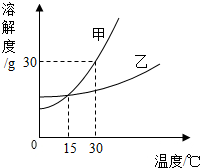 (2006?淄博)以下是同学们在学习溶液知识时实验报告中的部分内容,分析后请回答:
(2006?淄博)以下是同学们在学习溶液知识时实验报告中的部分内容,分析后请回答:| 试管编号 | 加入液体 | 加入物质 | 现象 |
| 1 | 10mL水 | 少量食盐 | 不溶 |
| 2 | 10mL乙醇 | 少量食盐 | 溶解 |
| 3 | 10mL水 | 几小粒碘 | 不溶 |
| 4 | 10mL乙醇 | 几小粒碘 | 溶解 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 水的质量(g) | 10 | 50 | 100 |
| KNO3的质量(g) | 3.2 | 15.8 | 31.6 |
| 温度(℃) | 20 | 40 | 60 |
| KNO3的质量(g) | 6.3 | 12.8 | 22.0 |
| 实验操作 | 实验现象和溶解程度 | 实验结果 |
| 取100mL水,加入25g硝酸钾,搅拌,恢复至20℃ | 全部溶解 | 得溶液① |
| 再加w g硝酸钾,搅拌,恢复至20℃ | 恰好饱和 | 得溶液② |
| 再加25g硝酸钾,搅拌,恢复至20℃ | 不溶解 | 得溶液③ |
| 加热 | 全部溶解 | 得溶液④ |
| 冷却至20℃ | 析出晶体a | 得溶液⑤ |
| 蒸发掉10g水,恢复至20℃ | 析出晶体b | 得溶液⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 溶解度(g/100g水) | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 | 246 |
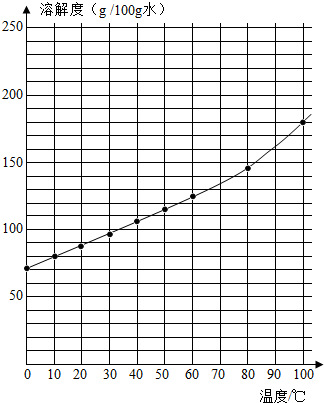 (2)根据溶解度曲线,小李设计了如下实验:
(2)根据溶解度曲线,小李设计了如下实验:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 以下是同学们在学习溶液知识时实验报告中的部分内容,分析后请回答:
以下是同学们在学习溶液知识时实验报告中的部分内容,分析后请回答:| 试管编号 | 加入液体 | 加入物质 | 现象 |
| 1 | 10mL水 | 少量食盐 | 不溶 |
| 2 | 10mL乙醇 | 少量食盐 | 溶解 |
| 3 | 10mL水 | 几小粒碘 | 不溶 |
| 4 | 10mL乙醇 | 几小粒碘 | 溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com