
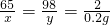
 ×100%=9.8%
×100%=9.8%

科目:初中化学 来源: 题型:
| 氯气的质量 | 漂白粉的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
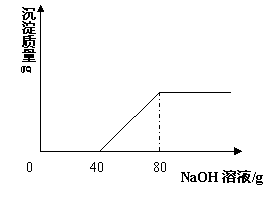
在一烧杯中盛有100 gCuSO4和H2SO4的混合溶液向其中逐渐滴加溶质质量分数为10%的NaOH溶液,混合溶液的质量与所滴入NaOH溶液的质量关系曲线如右图所示。请根据题意回答下列问题:
(1)在实验过程中产生沉淀的总质量是______ g。
(2)在实验过程中加入80 gNaOH溶液时所得溶液的pH是___ _7 (填“大于”“小于”或“等于”)。
(3)在实验过程中加入80 gNaOH溶液时,通过计算求此时所得不饱和溶液中溶质的质量分数。(计算结果精确至0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
在一烧杯中盛有100 gCuSO4和H2SO4的混合溶液向其中逐渐滴加溶质质量分数为10%的NaOH溶液,混合溶液的质量与所滴入NaOH溶液的质量关系曲线如右图所示。请根据题意回答下列问题![]() :
:
(1)在实验过程中产生沉淀的总质量是______ g。
(2)在实验过程中加入80 gNaOH溶液时所得溶液的pH是___ _7 (填“大于”“小于”或“等于
(3)在实验过程中加入80 gNaOH溶液时,通过计算求此时所得不饱和溶液中溶质的质量分数。(计算结果精确至0.1%)

查看答案和解析>>
科目:初中化学 来源: 题型:
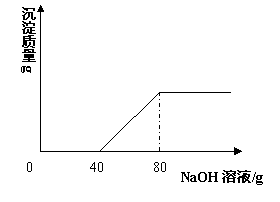
在一烧杯中盛有100 gCuSO4和H2SO4的混合溶液向其中逐渐滴加溶质质量分数为10%的NaOH溶液,混合溶液的质量与所滴入NaOH溶液的质量关系曲线如右图所示。请根据题意回答下列问题![]() :
:
(1)在实验过程中产生沉淀的总质量是______ g。
(2)在实验过程中加入80 gNaOH溶液时所得溶液的pH是___ _7 (填“大于”“小于”或“等于”)。
(3)在实验过程中加入80 gNaOH溶液时,通过计算求此时所得不饱和溶液中溶质的质量分数。(计算结果精确至0.1%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com