
����Ŀ����1����ˮɹ�οɵõ����κͿ�±�����п�±��ʳ�ε� ������͡������͡�����Һ�������� �����ÿ�±��ʯ���飮ϡ������Ƶ�Ӧ���ڷɻ�����ҵ�Ľ���þ�����з�����Ӧ�Ļ�ѧ����ʽ�Ǣ� ���� ���� ��
��2��һ���Ӻ�ˮ�л�õĴ��Σ����к�����������ɳ�Ȳ��������ʣ��ɲ������²����ȥ �� �� ������С��Ծ��������ᴿ�Ĵ��εijɷֽ���̽�����������ν�һ���ᴿ��
̽��һ����������л���ʲô���ʣ�
���ݺ�ˮ�ijɷݺͳ����ᴿ��ʵ����������ƴ����п��ܻ���������CaCl2��MgCl2������ʵ����֤�����Ʋ⣺ȡ�����ܽ⣬��������NaOH��Һ��Ŀ���Ǽ�����û�У���ѧʽ�� ����صķ�Ӧ����ʽΪ �������ټ�������Na2CO3��Һ��Ŀ���Ǽ�������û�У���ѧʽ�� ����صķ�Ӧ����ʽΪ ��ʵ��֤������������к��е�������CaCl2��
̽���������������NaCl�����������Ƕ��٣�
�����沽���������ʵ�飺�ٳ�ȡһ����������Ʒ���ڽ���Ʒ��ˮ�ܽ��Ƴɴ�����Һ�����������Һ�м������ij���Լ������ˣ��ܳ���ϴ�Ӻ�С�ĺ�ɵõ���������A������Һ�ڽ���ijһ�����������������������õ���������B������ʵ���еõ���ij�ֹ��壮
�ڢۢݲ����У���ʹ�õ�ͬһ�����������ƣ� ���ڲ���ں͢���ʹ������������������ͬ��������Ŀ�IJ�ͬ���ڲ�����е�Ŀ���� ���ڲ�����е�Ŀ���� ��������м����Լ��ǣ���ѧʽ�� ����ط�Ӧ����ʽΪ ������ݽ��еġ�ijһ�������� ��Ŀ���� ����ط�Ӧ����ʽΪ ��������У�����Ϊ��Ҫ�����Ĺ�����A����B�� ����A��B���㲻ѡ�������һ�ֹ���������� ��
���𰸡���1���ٿ�±��ʳ�εı�����Һ��
�ڱ��ͣ�������������ʳ�ξ��壬MgCl2��Ca��OH��2=Mg��OH��2����CaCl2��
Mg��OH��2��2HCl=MgCl2��2H2O��MgCl2![]() Mg��Cl2����
Mg��Cl2����
��2���ܽ⣬���ˣ�������
̽��һ����MgCl2��2NaOH=Mg��OH��2����2NaCl��
��MgCl2��MgCl2��2NaOH=Mg��OH��2����2NaCl��CaCl2��CaCl2+Na2CO3=CaCO3��+2NaCl��
̽�����������������ٴ��ε��ܽ⣻��ֹ���ھֲ��¶ȹ��ߣ����Һ�ηɽ���Na2CO3��CaCl2+Na2CO3=CaCO3��+2NaCl��
���������������ϡ���ᣬ��ȥ������̼���ƣ�Na2CO3+2HCl=2NaCl��H2O��CO2����
A��B�к��з�Ӧ���ɵ��Ȼ��ƣ�
����������1���ٿ�±�Ǻ�ˮŨ�����κ���������Ȼ��ƺ���С���ܹ�����������50%ʱ��ˮ��Һ���ں��������У���ˮ����������ɹ����Ũ��������ʳ�Σ���±ˮ�ﵽһ��Ũ��ʱ��28.5��30�����ȣ�������ɹ�Σ���±ˮ��Ϊ��±���ʿ�±��ʳ�εı�����Һ��
�ڿ�±�Ļ�ѧʽΪMgCl2��ʯ�������Ҫ�ɷ���Ca��OH��2����������Ϊ��MgCl2��Ca��OH��2=Mg��OH��2����CaCl2��Mg��OH��2��2HCl=MgCl2��2H2O��MgCl2![]() Mg��Cl2����
Mg��Cl2����
��2�������ᴿ�IJ���Ϊ���ٰѺ�����ɳ�Ĵ�ʳ����ȫ�ܽ⣻
�ڹ��˵�������ˮ����ɳ��
��������ˮ�֣����õ��Ȼ��ƾ��壮
̽��һ������Ϊ�Ȼ�þ���������Ʒ�Ӧ����������þ���������Ȼ������������Ʒ�Ӧû�г������������ɣ��ʼ�������NaOH��Һ��Ŀ���Ǽ�����û���Ȼ�þ���Ȼ�þ���������Ʒ�Ӧ�Ļ�ѧ����ʽΪ��MgCl2��2NaOH=Mg��OH��2����2NaCl��
����ΪNa2CO3��Һ��CaCl2��Ӧ����̼��Ƴ������ʼ�������Na2CO3��Һ��Ŀ���Ǽ�������û���Ȼ��ƣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��ijУѧ�����о�����ȼ�յ�����ʱ������������ʵ�飺��ȼһ֧��������ֱ���������ϣ����ձ���ס����ͼl��ʾ���������ݴ�ʵ��ش����⣺

������ȼ��ʱ���۲쵽�ձ��ڱڲ���ˮ����˵��ʯ���к��� Ԫ��
������Ϩ���˲�䣬�۲쵽��о�Ϸ�����һ�ư��̣����̵���Ҫ�ɷ��� ��
��2������ʦ��ָ���£�ͬѧ�����������������ⶨ������ȼ�չ��������������ı仯�������Ʋ��������ͼ2��ʾ��ʵ�飬�ó�����ͼ3��ʾ�����������ı仯��ͼ������ͼ3��ʾ������ͼ��ͬѧ�ǵó������½��ۣ�����˵����ȷ���� ����ţ�
A��ֻ�е������ľ�ʱ������Ż�Ϩ��
B������Ϩ��ʱ������ƿ����������
C������Ũ��С��һ��ֵʱ��������ȼ�գ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һʵ����ʵ������������ͭ��Һ��Ӧ��������ͭ���ɣ������н϶�����������Ϊȷ������ijɷ֣���������ʵ��̽����
������֪��SO2��ʹ���Ը��������Һ��ɫ�������ڼ��ȵ������¿ɻ�ԭ����ͭ��
��һ��̽�������������Ԫ�ؽǶȷ��������������SO2��O2��H2�е�һ�ֻ��֣�
������ʵ�飺
��1����ͬѧΪȷ���Ƿ���SO2����������ͨ�����Ը��������Һ�У���Һ��ɫδ�����仯����������� SO2����С����ޡ�����
��2����ͬѧ��Ϊֻ��O2������� �����飮ʵ��֤����ͬѧ�Ĺ۵㲻��ȷ��
��3����ͬѧΪ�ж��Ƿ���O2��ͬʱȷ������ɷ֣�ͨ���������ϵ�֪��O2+4KI+4HCl=2I2+4KCl+2H2O��I2Ϊ�ⵥ�ʣ�I2�����۱���ɫ���������������ͼ��ʾ��ʵ��װ�ã�
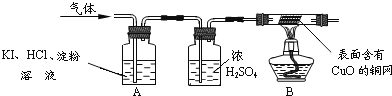
������ʵ����������ۣ�A�й۲쵽 ��֤����O2��B�й۲쵽 ��֤����������H2��
���ģ�ʵ�鷴˼�������Ϊ��ͬѧ�ڼ���֮ǰ��Ӧ�������� ��ȷ����ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ��������мס��ҡ��������������ʣ���һ�������³�ַ�Ӧ����÷�Ӧǰ������ʵ�����������ͼ��ʾ������˵����ȷ����

A���������ǵ���
B���ڸ÷�Ӧ�ж�һ��û�вμӻ�ѧ��Ӧ
C���÷�Ӧ�ǻ��Ϸ�Ӧ
D�����ҵ�����֮��һ���������ɱ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�С��ͬѧ�ü��Ȳ��ᾧ���Ƶõ�CO
��֪��H2C2O42H2O=CO��+CO2��3H2O����������ԭ��ʵ�������β���������������װ�ã�ͼ��ͼ�ң�
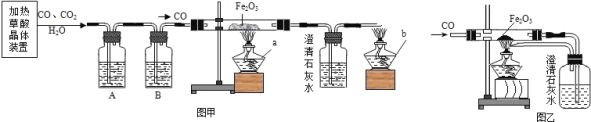
�ش��������⣺
��1���ڼ��ȷֽ���ᾧ���װ���У�������������ѡ��ʹ�ã�
���Թܢ��ձ��۾ƾ��Ƣ������������̨�������У������ܵ���Ƥ������ƿ
������Ҫ�õ��������� ������ţ�
��2��Ϊ�˻�ø��﴿����CO��A��B��װ����Ӧ�ֱ��� �� ��
��3��Ӳ�ʲ������з�����Ӧ�Ļ�ѧ����ʽ ��
��4��ѡ��ͼ�״���β����ʵ��ʱӦ�ȵ�ȼ ���a����b�������ľƾ��ƣ�ͼ����ͼ����ʾ��β������������Ƚϣ�����Ҫ�ŵ��� ��
��5���С���ͬѧͨ���������ϵ�֪�������£�CO�����Ȼ���PdCl2��Һ��Ӧ����������ѡ���˽�β��ֱ��ͨ���Ȼ�����Һ�н��д������÷�Ӧ�Ļ�ѧ����ʽΪ��CO+PdCl2+H2O=Pd��+CO2+2R������R�Ļ�ѧʽΪ ���˷�������������ȳ��˾���ͼ�ұ�ͼ����ʾ�������ŵ��⣬��ʵ��Ƕȿ������е��ŵ��� ��д��һ�������𰸼��ɣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��ѧ���ij��������ʣ�����A�ǵ��ʣ�B��C��E�������A��B��C��D��E����һ����ͬԪ�أ�����֮��Ĺ�ϵ��ͼ��ʾ����ͼ�С�������ʾ���˵������ܷ�����ѧ��Ӧ����������ʾ���ʼ����ת����ϵ����
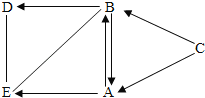
��1��C�Ļ�ѧʽΪ ��
��2��Bת��ΪD�Ļ�ѧ����ʽΪ ��E��D��Ӧ�Ļ�ѧ����ʽΪ ��
��3��Bת��ΪA�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������أ�KMnO4��������أ�K2MnO4������Ԫ�صĻ��ϼ۷ֱ���
A��+7��+6 B����7����6 C��+6��+5 D����6����5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���̼��̼���������˵���У�����ȷ����
A��C���Խ�CuO�е�Cu�û�������
B����һ��������CO2�ܹ�ת���CO��
C��CO��CO2������Ӧ�����κ�ˮ��
D�����ʯ��ʯī��C60����̼Ԫ�صĵ��ʡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڹ���ʱ������Ҫ�õ�һ�������ǣ� ��
A���������������ձ�
B���ձ���©����������
C����ƿ��©����������
D���Թܡ��ԹܼС��ձ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com