
【题目】我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献,工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质,现称取只含氯化钠杂质的纯碱样品11g,全部溶解在50g水中,当加入稀盐酸64.4g时,恰好完全反应,所得溶液的质量为121g。
试求:
(1)该纯碱样品的纯度(计算结果精确到0.1%)
(2)所得溶液中溶质的质量分数。
【答案】
(1)解:反应放出的CO2的质量为:64.4g+50g+11g-121g=4.4g
设参加反应的Na2CO3质量为x,生成的NaCl的质量为y
Na2CO3+ | 2HCl=2NaCl+H2O+ | CO2↑ |
106 | 117 | 44 |
x | y | 4.4g |
![]()
解之得x=10.6g
y=11.7g
碳酸钠纯度= ![]() ≈96.4%;
≈96.4%;
答:该纯碱样品的纯度约为96.4%;
(2)解:纯碱样品中NaCl的质量=11g-10.6g=0.4g
反应后溶液中NaCl的质量为=11.7g+0.4g=12.1g
反应后溶液中NaCl的质量分数= ![]() ×100%=10%
×100%=10%
答:所得溶液中溶质的质量分数为10%。
【解析】解:(1)反应放出的CO2的质量为:64.4g+50g+11g-121g=4.4g
设参加反应的Na2CO3质量为x,生成的NaCl的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
44 x 4.4g
![]() =
=![]() =
=![]()
解之得x=10.6g
y=11.7g
碳酸钠纯度=![]() ×100% ≈96.4%;
×100% ≈96.4%;
答:该纯碱样品的纯度约为96.4%;
(2)纯碱样品中NaCl的质量=11g-10.6g=0.4g
反应后溶液中NaCl的质量为=11.7g+0.4g=12.1g
反应后溶液中NaCl的质量分数=![]() ×100%=10%
×100%=10%
答:所得溶液中溶质的质量分数为10%.
所以答案是:(1)96.4%;10%.
【考点精析】关于本题考查的根据化学反应方程式的计算,需要了解各物质间质量比=系数×相对分子质量之比才能得出正确答案.


科目:初中化学 来源: 题型:
【题目】原子和分子都是微观粒子.
(1)原子不显电性原因是什么?
(2)如图所示,有A、B两只烧杯,在烧杯A中装入20mL蒸馏水,滴入2﹣3滴无色酚酞溶液,观察到杯中的溶液仍为无色.在烧杯B中装入10mL浓氨水,用一只大烧杯把A、B两只烧杯罩在一起,过几分钟后,发现烧杯A中的酚酞溶液变为红色,从这个实验中你得的结论是什么?(提示:浓氨水具有挥发性;酚酞溶液遇到浓氨水等碱性物质会变为红色)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在化学上物质结构决定物质的性质,而物质的性质又决定物质用途,请回答:
①氧气和液态氧都有助燃性的原因是_____;
②食品包装中用氮气来充气包装这是因为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列装置图回答问题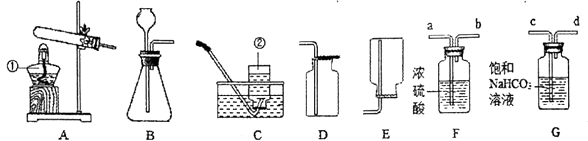
(1)图中标示仪器的名称是①②;
(2)欲使用高锰酸钾制取氧气,应选择的发生装装置是(填字母),反应原理用化学方程式表示为;为 , 应在试管口附近堵上一团棉花;若使用C装置收集氧气,实验结束时,应先从水槽中移出导气管,再熄灭酒糟灯,原因是。
(3)实验室制取二氧化碳气体时,发生装置可选择图中的(填装置编号),反应的化学方程式为。
(4)采用上述方法制取的二氧化碳中常含有氯化氢气体和水蒸气,为获得纯净、干燥的二氧化碳气体,可选用如图所示的F装置和G装置进行除杂和干燥,导管口连接的正确顺序是:
气体→()→()→()→()→D。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“电视之星18”是第21届俄罗斯足球世界杯的比赛用球。它是以甘蔗为原料首次制成环保型材料(三元乙丙橡胶)的足球。下列属于此材料化学性质的是( )
A. 耐磨损B. 抗氧化C. 绝缘性好D. 不易溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com