
| A. | 水结成冰前后,质量保持不变 | |
| B. | 红磷在氧气中燃烧生成固体的质量大于原来红磷的质量 | |
| C. | 50mL水与50mL酒精混合后总体积小于100mL | |
| D. | 4g碳与4g氧气反应,一定生成8g二氧化碳 |
分析 质量守恒定律是物质在发生化学变化中表现出来的一种规律,适用于化学变化;物质发生物理变化,则不适用于质量守恒定律来解释;是化学变化时也要对反应前后物质的质量关系进行计算判断,即反应时是否符合固定的质量比,据此分析解答即可.
解答 解:A、水加热变成水蒸气,是物理变化,不是化学变化,不符合质量守恒定律;故选项错误.
B、一定质量的红磷在空气中燃烧后,生成物的质量一定等于红磷与氧气的质量之和,生成固体的质量大于原来红磷的质量,故选项正确.
C、50mL水和50mL酒精混合后总体积不等于100mL,是因为分子间有间隔,此变化为物理变化,不符合质量守恒定律;故选项错误.
D、碳和氧气反应的化学方程式为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2可知,碳、氧气、二氧化碳的质量比为3:8:11,故4g碳与4g氧气反应,不生成8g二氧化碳,故选项错误.
故选B.
点评 本题难度不大,考查的是质量守恒定律的应用,理解质量守恒定律并能灵活运用是正确解答本题的关键.


 科学实验活动册系列答案
科学实验活动册系列答案科目:初中化学 来源:2017届江苏省扬州市江都区五校联谊九年级下学期第二次模拟考试化学试卷(解析版) 题型:选择题
右图是NaCl、MgSO4、KCl固体的溶解度曲线,下列说法正确的是
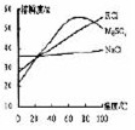
A、60℃三种物质的饱和溶液中,溶质质量分数最大的是KCl溶液
B、将80℃不饱和的MgSO4溶液降温至40℃,一定能得到其饱和溶液
C、40℃时MgSO4的溶解度比NaCl小
D、将80℃含有少量NaCl的KCl饱和溶液降温至20℃,可得到KCl晶体
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2:17 | B. | 1:3 | C. | 3:5 | D. | 4:9 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
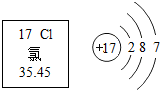
| A. | 氯的原子序数为17 | |
| B. | 氯原子核外有3个电子层 | |
| C. | 氯的相对原子质量为35.45 | |
| D. | 在化学反应中,氯原子容易失去最外层电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验标号 药品 | 甲 | 乙 | 丙 | 丁 |
| 大理石(m0g) | 块状 | 块状 | 粉末状 | 粉末状 |
| 盐酸(过量) | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
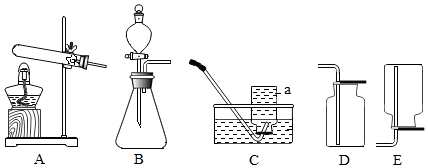
| 实验目的 | 原料 | 发生装置 | 主要原因 |
| 制取氧气 | 粉末状二氧化锰和稀过氧化氢溶液 | B |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
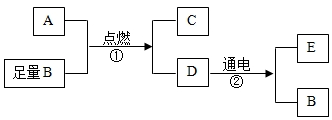
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com