
| A. | 铁钉锈蚀实验 | |
| B. | 用注射器探究空气与水哪种物质易被压缩 | |
| C. | 探究影响物质溶解性因素的实验 | |
| D. | 氢氧化钠溶液的酚酞试液中滴加稀盐酸探究中和反应 |
分析 只有比较才有鉴别,所以对比实验可通过若干个装置同时探究一个或多个条件对同一事件的影响,其关键是必须至少有一组作为对照.
解答 解:A、铁钉锈蚀的实验必须通过在不同的环境中来比较而得出其锈蚀的条件,故A属于对比实验;
B、用注射器来探究空气和水哪种更易被压缩,是探究同一装置对不同物种的比较,故B属于对比实验;
C、探究影响物质溶解性因素的实验,可通过温度、溶质、溶剂的种类等对照项进行实验并分析结果,是对比实验,故C属于对比实验;
D、中和反应是指酸和碱之间的反应,所以通过氢氧化钠和稀盐酸的反应,仅仅是对该反应类型进行验证,不存在对比,故D不属于对比实验.
故选D.
点评 对比实验是运用比较的方法来提示事物的性质或变化规律的一种实验方法,再设计实验时要了解其原理和区别,这样在设计实验或评价实验时,才会有针对性.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:初中化学 来源: 题型:选择题
| A. | HCl、NaOH、H2SO4 | B. | AgNO3、HNO3、BaCl2 | ||
| C. | FeCl3、Na2SO4、KNO3 | D. | CuSO4、NaCl、KOH |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 某白色固体与熟石灰混合后加热,产生可使湿润的红色石蕊试纸变蓝色的气体,证明该固体是铵盐 | |
| B. | 向某无色溶液中滴入酚酞试液,呈红色,证明该溶液是碱溶液 | |
| C. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 | |
| D. | 搅拌能加快蔗糖在水中的溶解,其原因是增大了蔗糖的溶解度 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 合成纤维的吸水性和透气性比纯羊毛好 | |
| B. | 这种“披肩”不宜用碱性强的洗涤剂清洗 | |
| C. | 二毛皮的纤维可用燃烧法鉴别是否属于天然纤维 | |
| D. | 羊毛的主要成分为蛋白质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
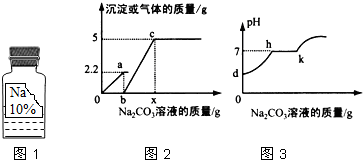 实验室有一瓶保管不当的试剂(如图1),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
实验室有一瓶保管不当的试剂(如图1),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加氢氧化钙溶液 | 白色浑浊 | 猜想②正确 相关的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com