
【题目】右图A、B、C三种固体物质的溶解度曲线。
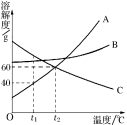
(1)t1℃时,A物质的饱和溶液中溶质的质量分数是 。
(2)使t1℃时C物质的不饱和溶液都变成饱和溶液,采用的方法是 (写一条)。
(3)t2℃时,B物质的溶解度 C物质的溶解度(填“大于”、“小于”或“等于”)。
科目:初中化学 来源: 题型:
【题目】下图所示为实验室中常见的气体制备和收集装置。
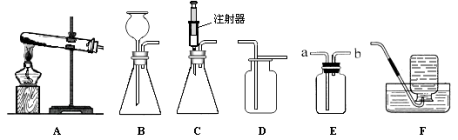
请回答下列问题:(1)实验室用高锰酸钾制取氧气,应选用发生装置 (填字母序号),反应的文字表达式为 。若用装置D收集氧气,验满的方法是 。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的优点是 。
(3)欲使用装置E用排空气法收集密度比空气大的二氧化碳,则气体应从 (填“a”或“b”)端通入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从 (填“a”或“b”)端通入。
(4)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置 (填字母序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】研究和控制化学反应条件有重要意义。
(1)同学们想探究双氧水的浓度对反应速率的影响。在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间。
实验 | 双氧水的质量(g) | 双氧水浓度(%) | 二氧化锰质量(g) | 收集时间(s) |
1 | 50 | 6 | 5 | 200 |
2 | 50 | 12 | 5 | 100 |
3 | 50 | 18 | ______ | 67 |
①写出上述反应的文字表达式________________________。
②实验3中,加入的二氧化锰质量为___________g。
③相同条件下,实验3产生氧气的速率最快,说明________________________。
④同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气。
为了验证加热双氧水也可以产生氧气,同学们选择右图装置(气密性良好)进行实验。实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是________________,同学分析原因后,采用了____________法收集气体,再检验,证明加热双氧水也可产生氧气。
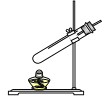
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙是探究氧气化学性质时三个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题.
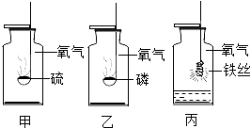
(1)所发生的三个反应有多个共同的特点,分别是:① ;② ;③ .
(2)丙实验进行时,发生反应的文字表达式为 ,甲瓶底为什么要放少量的水? .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用下列装置来制取氧气:
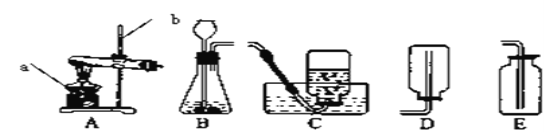
(1)写出图中有标号仪器的名称:a 、b 。
(2)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是 (填序号),其中二氧化锰起 作用。
(3)用E装置收集氧气的依据是 ,检验氧气是否集满的方法是 。
(4)用排水法开始收集氧气的适宜时刻是 。
(5)用排水法收集氧气完毕后,应先 ,后 ,原因是 。
(6)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小。NH3极易溶于水。制取并收集NH3,应该从上图中选择的是 和 (填序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合下列实验常用装置,回答有关问题.
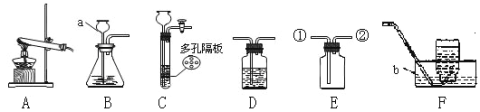
(一)(1)若用B、F组成制取某气体的装置,写出制取此气体的化学方程式为 ,若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,并在该装置中盛放 试剂(填写试剂名称).如果用E装置收集该气体则气体从 端进入(填“①”或“②”)。
(2)乙炔(C2H2)是无色、无味、易燃的气体,乙炔的密度比空气略小,难溶于水。乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体)与水反应生成,同时生成一种白色固体。已知碳化钙与水反应非常剧烈。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置是 。
(二)实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示).
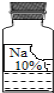
小强和小华同学很感兴趣,决定对其成分进行探究.
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ初中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3.
ⅡNa2CO3和NaHCO3的水溶液都呈碱性.
Ⅲ室温(20℃)时,测定四种物质的溶解度数据如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度g | 36 | 109 | 215 | 9.6 |
小华根据试剂瓶标注的质量分数为10%和上表中的溶解度数据判断,这瓶试剂不可能是
【作出猜想】①可能是NaCl;②可能是Na2CO3;③可能是
【实验探究】
(1)小强用洁净的玻璃棒蘸取试液于pH试纸上,测得pH>7,则这瓶试剂不可能是
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验.
实验步骤 | 实验现象 | 结论及化学方程式 |
取少量溶液于试管中,滴加 | 产生大量气泡 | 反应的化学方程式: |
② 把产生的气体通入澄清的石灰水中. | 澄清的石灰水变浑浊 | 猜想②正确. 反应的化学方程式: |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学教材 “寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【提出问题】(1)氧化铁能否作过氧化氢溶液分解的催化剂?
(2)氧化铁与二氧化锰催化效果哪个好?
【实验探究】
实验步骤 | 实验现象 |
①分别量取5 mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入a g氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象。 | A试管中产生大量气泡,带火星木条复燃,B试管中的现象 |
②待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管内,如此反复多次实验,观察现象。 | 试管中均产生大量气泡,带火星木条均复燃 |
③将实验②中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为a g。 | |
④分别量取5 mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入a g氧化铁粉末,向D试管中加入a g二氧化锰粉末,观察现象。 |
|
(1)A中产生的气体是 ;B试管中的现象 。
(2)实验②、③证明:氧化铁的 和 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(3)写出氧化铁催化过氧化氢分解的文字表达式 。
(4)实验设计④的目的是 ,若实验④观察到D试管中产生气泡的速率更快,由此你可以得到的结论是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为哈药集团制药厂生产的“新盖中盖牌”高钙片标签上的部分文字,请仔细阅读后回答下列问题。

(1)“新盖中盖牌”高钙片中的“钙”应理解为(填编号)
①元素 ②原子
③分子 ④氧化物
(2)维生素D种类较多,其中维生素D2的化学式为C28H44O,维生素D2的相对分子质量是 。②维生素D2中碳、氢、氧三种元素质量比是 。
(3)计算高钙片中碳酸钙的质量分数是多少?
友情提示:(物质的质量分数=该物质的质量/总物质的质量×100﹪)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com