
分析 根据氢氧化钠的质量求算和氢氧化钠反应消耗的盐酸以及生成的氯化钠的质量,然后根据和碳酸钠反应的盐酸的质量求算碳酸钠的质量和生成的氯化钠的质量,进而求算对应的质量分数.
解答 解:设和氢氧化钠反应的HCl的质量为x,生成的氯化钠的质量为y
NaOH+HCl=NaCl+H2O
40 36.5 58.5
4g x y
$\frac{40}{4g}$=$\frac{36.5}{x}$=$\frac{58.5}{y}$
x=3.65g
y=5.85g
则HCl的总质量为7.3%×l00g=7.3g
则和碳酸钠反应的HCl的质量为7.3g-3.65g=3.65g
设碳酸钠的质量为z,生成的氯化钠的质量为a,生成的二氧化碳的质量为b
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
z 3.65g a b
$\frac{106}{z}$=$\frac{73}{3.65g}$=$\frac{117}{a}$=$\frac{44}{b}$
z=5.3g
a=5.85g
b=2.2g
样品中碳酸钠的质量分数为$\frac{5.3g}{10g}$×100%=53%
最后所得溶液中溶质的质量分数为$\frac{5.85g+5.85g}{5.3g+100g+96.9g-2.2g}$×100%=5.85%
答:(1)100g质量分数为7.3%的盐酸中,溶质氯化氢的质量为 7.3g;
(2)样品中碳酸钠的质量分数53%.
(3)最后所得溶液中溶质的质量分为5.85%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


科目:初中化学 来源: 题型:选择题
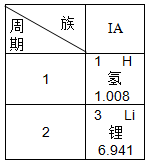
| A. | 锂原子的原子序数为3 | B. | 氢元素的核外电子数是1 | ||
| C. | 锂元素和氢元素都属于金属元素 | D. | 锂元素和氢元素属于同周期元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
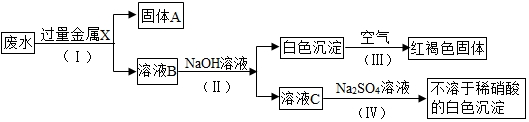
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
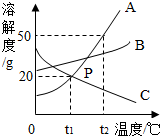 根据如图所示的物质溶解度曲线图,回答以下问题:
根据如图所示的物质溶解度曲线图,回答以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
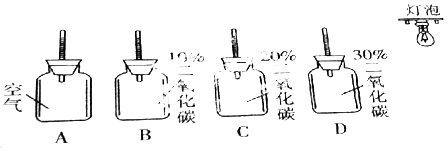
| 温度计标号 | A | B | C | D |
| 初始温度 | 180C | 180C | 180C | 180C |
| 10分钟后温度 | 200C | 210C | 220C | 230C |
| 避光保存10分钟后的温度 | 18.50C | 19.50C | 210C | 22.50C |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com