
从HCl、NaCI、NaOH、Na2CO3、Ca(OH)2几种溶液中取出其中的两种混合,可能的组合共有_____________种。
(1)若混合后溶液质量减小,可能的组合是_____________、_____________。
(2)若混合后溶液质量不变,但发生了化学反应,有关的化学方程式为:
______________________________________________________________________________
______________________________________________________________________________
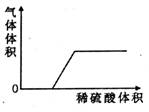
(3)将稀硫酸逐滴滴入剩下的几种组合中,若产生气体与加入稀硫酸有如下图所示的关系,则这样的组合可能是____________________________________________________。
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源:邵阳 题型:问答题
查看答案和解析>>
科目:初中化学 来源:2005年湖南省邵阳市中考化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com