
| ||
| ||
| ||
| 16 |
| 30aKg |
| 44 |
| x |


科目:初中化学 来源: 题型:
| A、水是由氢元素和氧元素组成的 |
| B、正极端产生的气体能使带火星的木条复燃 |
| C、负极端产生的气体能燃烧 |
| D、正极端与负极端产生的气体体积比约为2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 我市某校开展了以保护大气环境为主题的调查研究活动.下列是某综合实践活动小组的部分研究报告,请加以完善.
我市某校开展了以保护大气环境为主题的调查研究活动.下列是某综合实践活动小组的部分研究报告,请加以完善.查看答案和解析>>
科目:初中化学 来源: 题型:
 同学们在学习Ca(OH)2的化学性质时,对Ca(OH)2溶液和Na2CO3溶液反应后过滤得到的滤液的成分进行探究.请你一同探究并回答下列问题:
同学们在学习Ca(OH)2的化学性质时,对Ca(OH)2溶液和Na2CO3溶液反应后过滤得到的滤液的成分进行探究.请你一同探究并回答下列问题:| 实验操作 | 预期现象和结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:

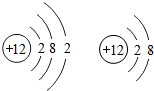 表示一种元素的两种粒子,它们属于同一种元素的依据是
表示一种元素的两种粒子,它们属于同一种元素的依据是查看答案和解析>>
科目:初中化学 来源: 题型:
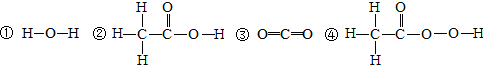
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、C粉(CuO)→稀盐酸 |
| B、CaCl2溶液(HCl)→碳酸钙粉末 |
| C、CO2气体(H2O)→生石灰 |
| D、CO气体(CO2)→氢氧化钠溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com