
(3分)用作牙膏摩擦剂的轻质碳酸钙,工业上常用石灰石来制备,主要生产流程如下:
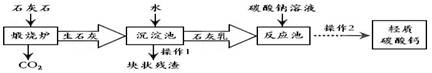
(1)投入到“反应池”中的石灰乳是混合物,属于 (选填:溶液、悬浊液或乳浊液)。
(2)若在化学实验室里分离“反应池”中的混合物,该操作的名称是 。
(3)本流程图中 (物质)可以替代“碳酸钠溶液”达到降低生产成本和节能减排。
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
| 儿童牙膏 | 防臭牙膏 | 透明牙膏 | |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
| 物质的类别 (指酸、碱、盐、氧化物) |
碱 碱 |
盐 | 氧化物 氧化物 |
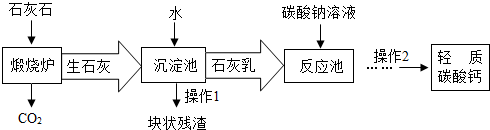
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
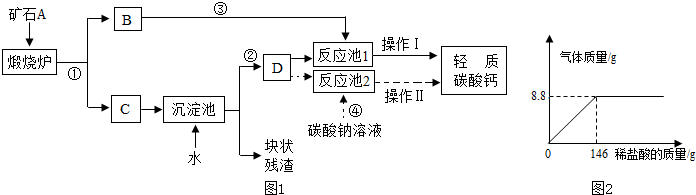 请回答下列问题:
请回答下列问题:
| ||
| ||
| 100 |
| 44 |
| X |
| 8.8g |
| 73 |
| 44 |
| Y |
| 8.8g |
| 20g |
| 25g |
| 14.6g |
| 146g |
| 100 |
| 44 |
| X |
| 8.8g |
| 73 |
| 44 |
| Y |
| 8.8g |
| 20g |
| 25g |
| 14.6g |
| 146g |
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
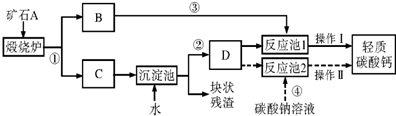
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com