

分析 (1)氢氧化钠溶液显碱性,pH大于7,能和稀盐酸反应生成氯化钠和水,氯化钠溶液显中性,不能使酚酞试液变色;
(2)根据图中信息可以判断相关方面的问题;
(3)氢氧化钠能和二氧化碳反应生成碳酸钠和水,稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳;
(4)根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)由图可知溶液的pH由大于7逐渐减小,说明甲同学将稀盐酸溶液加入到另一溶液中;
若原溶液中滴有酚酞试液,B点时稀盐酸和氢氧化钠恰好完全反应,对应的实验现象是溶液由红色变成无色.
故填:稀盐酸;溶液由红色变成无色.
(2)根据温度随pH变化的图象,该反应属于放热反应.B点比A点温度低的原因是:A点时恰好完全反应,放热最多,完全反应后溶液散热,温度降低.
故填:放热;A点时恰好完全反应,放热最多,完全反应后溶液散热,温度降低.
(3)丙组同学用另一瓶久置的氢氧化钠溶液进行上述实验时,发现有少量的气泡冒出,是因为稀盐酸和碳酸钠反应生成了二氧化碳,产生气泡反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
若另取该溶液,滴加酚酞试液变红,不能说明该氢氧化钠溶液为部分变质,这是因为氢氧化钠溶液和碳酸钠溶液都是显碱性溶液,都能够使酚酞试液变红色.
故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑;不能.
(4)设废水中氯化氢质量为x,
氢氧化钠质量为:20g×20%=4g,
NaOH+HCl═NaCl+H2O,
40 36.5
4g x
$\frac{40}{4g}$=$\frac{36.5}{x}$,
x=3.65g,
废水中氯化氢的溶质质量分数为:$\frac{3.65g}{100g}$×100%=3.65%,
答:废水中氯化氢的溶质质量分数为3.65%.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 单质是由一种元素组成的,因此由一种元素组成的纯净物一定是单质 | |
| B. | 中和反应一定有盐生成,则有盐生成的反应一定是中和反应 | |
| C. | 分子是构成物质的微粒,因此物质都是由分子构成的 | |
| D. | 氧化物中含有氧元素,因此含有氧元素的化合物一定是氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
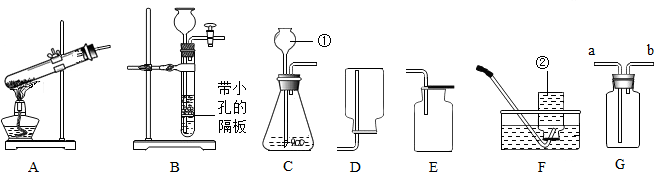
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图所示,烧杯内盛有水,瓶中X为固体,当把滴管内的液体Y滴入瓶中,烧杯内导管口一定没有气泡冒出的是 ( )
如图所示,烧杯内盛有水,瓶中X为固体,当把滴管内的液体Y滴入瓶中,烧杯内导管口一定没有气泡冒出的是 ( ) | A | B | C | D | |
| X | Na2CO3 | NH4NO3 | NaOH | Zn |
| Y | HCl | H2O | H2O | H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

 所表示的粒子符号为S,它的最外层电子数为6.
所表示的粒子符号为S,它的最外层电子数为6.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 实验小组同学欲利用氢氧化钠溶液与硫酸探究中和反应中的热量变化.请你参与探究实验.
实验小组同学欲利用氢氧化钠溶液与硫酸探究中和反应中的热量变化.请你参与探究实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com