
| 实验步骤 | 实验现象 | 结 论 |
| 取样品,滴加盐酸 | 产生大量气泡 | 氢氧化钠已变质 |


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:阅读理解

| ||
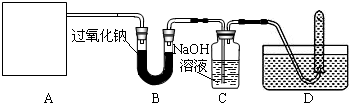
| 实验步骤 | 实验现象 | 实验结论及方程式 |
| ①取少量A中反应后的固体于试管中; ② ③ |
② ③ |
反应后生成的固体是碳酸钠,写出步骤③的方程式 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实 验 操 作 | 实 验 现 象 | 结 论 |
| 取少量白色粉末 滴加稀盐酸 |
有 气体 生成 |
乙同学认为自己的猜想正确. 反应的方程式为: Na2CO3+2HCl=2NaCl+CO2↑+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:
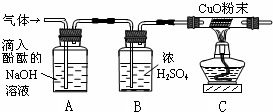
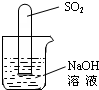 (2)小组内一同学又设计了判断SO2与NaOH溶液能否发生反应的装置(如右图),实验时发现试管内液面上升,就得出SO2与NaOH溶液发生反应的结论,其他同学认为这一结论不严谨,理由是
(2)小组内一同学又设计了判断SO2与NaOH溶液能否发生反应的装置(如右图),实验时发现试管内液面上升,就得出SO2与NaOH溶液发生反应的结论,其他同学认为这一结论不严谨,理由是查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com