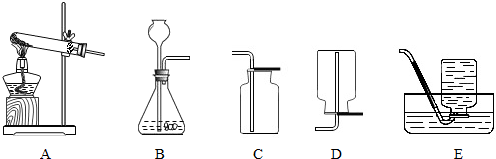
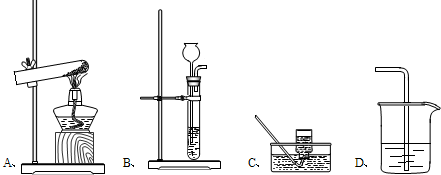
解:(1)加热高锰酸钾制取氧气试管口要放棉花,故该装置是用加热氯酸钾、二氧化锰作催化剂制取氧气,同时生成氯化钾,方程式是:2KClO
3
2KCl+3O
2↑;氧气的密度比空气大,不易溶于水,可用向上排空气或排水法收集;利用二氧化锰作催化剂、分解过氧化氢溶液制取氧气可用B装置,同时生成水,方程式是:2H
2O
2
2H
2O+O
2↑;
(2)实验室制取二氧化碳:碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,方程式是:CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;该反应不需加热,属于固体和液体常温反应,故选发生装置B,二氧化碳的密度比空气大且能溶于水,故只能用向上排空气收集;检验二氧化碳是否收集满用燃着的木条放于集气瓶口,观察木条是否熄灭;
(3)草酸是一种固体,实验室常用加热使其分解的方法来制取一氧化碳气体,属于固体加热型,故选发生装置A,一氧化碳的相对分子质量为28,与空气的平均相对分子质量29非常接近,故不宜用排空气法收集,一氧化碳难溶于水,可用排水法收集;
(4)用固体甲和液体乙反应来制取气体丙,不需加热,属于固液常温型,故选发生装置B;收集气体丙时只能用E装置,则可推知丙的性质可能有不(不易)溶于水、不与水反应、密度与空气接近或能与空气中的某气体反应.
故答案为:
(1)2KClO
3
2KCl+3O
2↑;D或E;2H
2O
2
2H
2O+O
2↑
(2)CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;B;D;将燃着的木条放在集气瓶口,火焰立即熄灭,说明已满;
(3)A;E;
(4)B;不(不易)溶于水;不与水反应;密度与空气接近或能与空气中的某气体反应.
分析:(1)A装置是用加热固体的方法制取氧气,且试管口无棉花,据此分析所用药品,书写方程式;并据氧气的密度和溶解性选择收集装置;B装置适用于固液混合常温反应制取气体,据此分析解答;
(2)根据实验室制取二氧化碳的反应原理书写方程式,并据发生和收集装置的选取依据和二氧化碳的制法、性质分析解答;检验二氧化碳是否收集满用燃着的木条放于集气瓶口,观察木条是否熄灭;
(3)根据反应物的状态和反应条件选择发生装置,依据一氧化碳的密度和溶解性选择收集装置;
(4)依据发生装置和收集装置的选取方法分析解答.
点评:本题主要对装置的选取方法进行了细致的考查和应用,并考查了验满、反应方程式的书写,通过解答本题很好的培养了学生对知识的掌握及灵活应用能力.

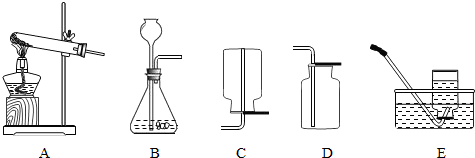
 2KCl+3O2↑;氧气的密度比空气大,不易溶于水,可用向上排空气或排水法收集;利用二氧化锰作催化剂、分解过氧化氢溶液制取氧气可用B装置,同时生成水,方程式是:2H2O2
2KCl+3O2↑;氧气的密度比空气大,不易溶于水,可用向上排空气或排水法收集;利用二氧化锰作催化剂、分解过氧化氢溶液制取氧气可用B装置,同时生成水,方程式是:2H2O2 2H2O+O2↑;
2H2O+O2↑; 2KCl+3O2↑;D或E;2H2O2
2KCl+3O2↑;D或E;2H2O2 2H2O+O2↑
2H2O+O2↑

 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案