
分析 (1)据常用仪器回答;
(2)用过氧化氢制取少量氧气时,属于固液常温型,反应容器可选试管,故可选发生装置C,氧气不易溶于水、密度比空气大,故可用排水法、向上排空气法收集,并据反应原理书写文字表达式,结合装置特点分析解答;
(3)加热高锰酸钾制取氧气属于固体加热型,故选发生装置D,并据反应原理书写文字表达式;
(4)验满氧气的方法为:将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
(5)据铁丝燃烧现象和注意事项解答;
(6)用注射器C检查装置E的气密性时,向锥形瓶中加入少量水至浸没长颈漏斗下端,将注射器C连接到装置E的导管口处,缓慢拉动注射器C的活塞,观察现象;
(7)用装置E制取CO2时,如用注射器C替换长颈漏斗,优点是可以控制反应的速率;
(8)据排水法收集氧气分析解答;
(9)实验室加热高锰酸钾制取氧气时,试管口应放一团棉花,以防止加热时高锰酸钾粉末进入导管;铁丝在氧气中燃烧的实验,失败的原因有:氧气浓度太低、铁丝太粗、表面的锈未除去,据此进行分析解答.
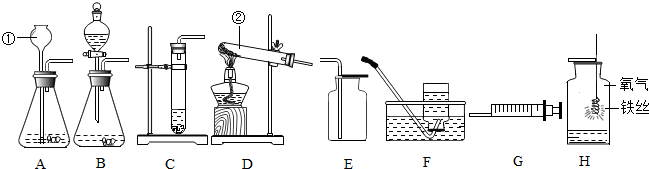
解答 解:(1)标号仪器是长颈漏斗、试管;
(2)用过氧化氢制取少量氧气时,属于固液常温型,反应容器可选试管,故可选发生装置C,氧气不易溶于水、密度比空气大,故可用排水法、向上排空气法收集;
如需随时控制生产气体的量并节约药品,发生装置最好选用B,因为分液漏斗可控制液体的滴加速率,进而可控制产生气体的量,不需氧气时不再滴加,可节约药品;反应的文字表达式是:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
(3)加热高锰酸钾制取氧气属于固体加热型,故选发生装置D,反应的文字表达式是:高锰酸钾$\stackrel{加热}{→}$锰酸钾+氧气+二氧化锰;
(4)验满氧气的方法为:将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
(5)如图H,铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,而瓶底预先放入少量水,是为了防止燃烧生成的高温熔融物溅落炸裂瓶底;
(6)用注射器C检查装置E的气密性时,向锥形瓶中加入少量水至浸没长颈漏斗下端,将注射器C连接到装置E的导管口处,缓慢拉动注射器C的活塞,锥形瓶内压强减小,在大气压强的作用下,水长颈漏斗中的水面下降,长颈漏斗下端有气泡逸出,表示装置E的气密性良好;
(7)注射器与长颈漏斗比较,注射器上有可以控制的活塞,可以根据实验时的需要添加药品,不用时可随时停止,所以用装置E制取CO2时,如用注射器C替换长颈漏斗,优点是可以控制反应的速率;
(8)若用装置F收集的氧气不纯,其原因可能是:集气瓶内未装满水留有气泡,或有气泡冒出就立即收集,使收集的氧气中混入了空气;
(9)小林用高锰酸钾制取并收集了一瓶氧气,呈浅红色,可能是因为在试管口没有放一团棉花,导致加热时高锰酸钾粉末进入导管;
在做细铁丝燃烧实验时,未见细铁丝燃烧,可能是集气瓶内氧气的浓度太低,不足以使铁丝燃烧或剧烈燃烧、火星四射;导致氧气的浓度低的原因有:用排水法收集氧气时,没等导管口气泡连续均匀的产生时就收集;可能未等火柴燃烧尽就插入盛氧气的集气瓶中,火柴继续燃烧消耗了一定量的氧气,同时有大量的热量放出,使瓶内氧气膨胀逸出;也可能是铁丝表面生锈了而未打磨除去(合理即可);
为防止防止生成物熔化溅落下来炸裂集气瓶,集气瓶底预先铺上一层细沙或放少量的水,故小红实验出现的问题为:没有预先在集气瓶的底部放少量的水或沙子;
故答案为:
(1)长颈漏斗; 试管;
(2)C; E(或F); B; 过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;
(3)D;高锰酸钾$\stackrel{加热}{→}$锰酸钾+氧气+二氧化锰;
(4)将带火星的木条放于集气瓶口,若木条复燃则满;
(5)火星四射; 防止燃烧生成的高温熔融物溅落炸裂瓶底;
(6)①浸没长颈漏斗下端; ③长颈漏斗口下端有气泡冒出;
(7)可以控制反应速率;
(8)集气瓶未装满水; 未等气泡连续、均匀冒出就开始收集;
(9)小林:试管口没有塞棉花; 铁丝表面生锈了而未打磨除去(合理均可);
小红:没有预先在集气瓶的底部放少量的水或沙子.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了文字表达式的书写,实验注意事项、铁丝燃烧实验等知识,综合性比较强,知识容量大.掌握相关知识并能结合题意灵活解答是解决问题的关键.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:填空题
 取一块金属钠,用小刀切下一小块.观察到切面呈银白色,切面很快变暗,这是由于钠极易跟空气中的氧气反应生成氧化钠.把一小块金属钠投入盛有水的烧杯中,钠浮在水面上,钠与水迅速反应生成氢氧化钠和氢气,放出的热使钠熔成小球,小球在水面上滚动,发出“嗤嗤”的声响,小球越来越小,最后完全消失.
取一块金属钠,用小刀切下一小块.观察到切面呈银白色,切面很快变暗,这是由于钠极易跟空气中的氧气反应生成氧化钠.把一小块金属钠投入盛有水的烧杯中,钠浮在水面上,钠与水迅速反应生成氢氧化钠和氢气,放出的热使钠熔成小球,小球在水面上滚动,发出“嗤嗤”的声响,小球越来越小,最后完全消失.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化学变化和化学反应是同一个概念 | |
| B. | 物质发生化学变化时一定同时发生物理变化 | |
| C. | 化学变化的特征就是有新物质生成 | |
| D. | 有发光放热等现象的变化一定是化学变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 为了节约药品,将用剩的药品放回原试剂瓶 | |
| B. | 酒精灯打翻着火,用湿抹布扑盖 | |
| C. | 玻璃仪器用水冲洗三遍就可以 | |
| D. | 药品直接放在天平托盘上称重 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 结论 |
| 1、取适量过氧化钠放入盛有水的烧杯中 | 固体溶解得无色溶液有能使带火星的木条复燃的气体生成. | 有氧气生成 |
| 2、向所得溶液中滴入硫酸铜溶液 | 有蓝色沉淀生成 | 过氧化钠能(填能否)与水反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 小兵在一本参考书上发现,镁居然能在二氧化碳气体中燃烧!于是他迫不及待地做起了这个实验:将镁条点燃后迅速伸入盛二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种白色粉末和一种黑色粉末.
小兵在一本参考书上发现,镁居然能在二氧化碳气体中燃烧!于是他迫不及待地做起了这个实验:将镁条点燃后迅速伸入盛二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种白色粉末和一种黑色粉末.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 ”表示氧原子,“
”表示氧原子,“ ”表示氢原子)
”表示氢原子)
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子、原子、离子都是构成物质的微粒 | |
| B. | 分子是由原子构成的 | |
| C. | 带电的原子或原子团叫离子 | |
| D. | 分子、原子、离子都是带电的微粒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com