
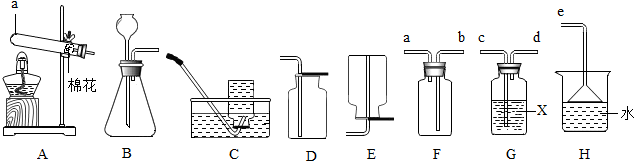
分析 (1)据常用仪器回答;
(2)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,故选固液常温型的发生装置,二氧化碳能够溶于水,密度比空气大;
(3)高锰酸钾受热时分解生成锰酸钾、二氧化锰和氧气,据此书写方程式;
(4)收集一瓶干燥的SO2,则须先将气体干燥,再收集,因为二氧化硫有毒、易溶于水,还要对尾气进行吸收处理,浓硫酸具有吸水性,可以用作某些气体的干燥剂.
解答 解:(1)仪器a是作为反应容器的试管;
(2)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,故选固液常温型的发生装置B,二氧化碳能够溶于水,密度比空气大,所以用向上排空气法收集;
(3)高锰酸钾受热时分解生成锰酸钾、二氧化锰和氧气,反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)收集一瓶干燥的SO2,则须先将气体干燥,再收集,因为二氧化硫有毒、易溶于水,还要对尾气进行吸收处理;所以要通过c导管把二氧化硫导入盛有浓硫酸的试剂瓶中进行干燥,通过d导管导出后,因为二氧化硫密度比空气大,所以通过b导管导入集气瓶中收集,为了防止二氧化硫逸出扩散到空气中污染环境,应该把a导管连接到e导管上,通过水吸收逸出的二氧化硫;
故答案为:(1)试管;
(2)BD;
(3)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)c→d→b→a→e.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,洗气装置中导管要长进短出,双导管收集密度比空气大的气体,应从长导管进气,短导管便于排尽空气,发生装置据反应物的状态和反应条件进行选择,收集装置据气体的密度和溶解性进行选择.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
| 序号 | ① | ② | ③ | ④ |
| 物质 | 醋酸 | 水 | 熟石灰 | 小苏打 |
| 化学式 | CH3COOH | H2O | Ca(OH)2 | NaHCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 硝酸铵[NH4NO3]是农业上常用的一种氮肥,用来为植物提供所需的氮元素.
硝酸铵[NH4NO3]是农业上常用的一种氮肥,用来为植物提供所需的氮元素.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Ba(NO3)2→BaSO4 | B. | H2SO4→HCl | C. | CuO→Cu(OH)2 | D. | Ba(OH)2→Fe(OH)3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲烷 | B. | 镁 | C. | 硫 | D. | 铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | KCl | NH4Cl | CaCl2 | ① |
| 现象 | 继续发生反应生成二氧化碳气体,但反应较慢,反应一段时间后就趋于停止. | CaCl2溶解并生成大量的白色固体,但不能继续发生反应 | 没有明显 可见的现象 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com