
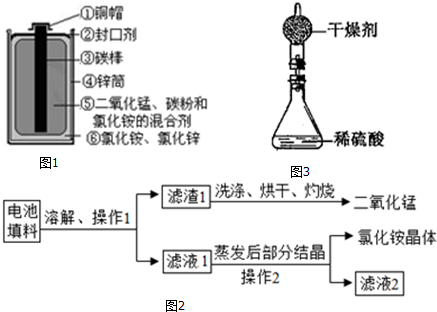
| 实验编号 | 试剂 | 前10 min 内产生的氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
| a | 纯锌 | 30 mL 30% | 564.3 |
| b | 含杂质的锌 | 30 mL 30% | 634.7 |
| c | 纯锌 | 30 mL 20% | 449.3 |
| d | 纯锌 | 40 mL 30% | 602.8 |
| 反应前 | 充分反应后装置及反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌皮质量 | |
| 342.1g | 16g | 357.7g |
| 65 |
| 2 |
| x |
| 0.4g |
| 13g |
| 16g |


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
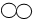 ”和“
”和“ ”分别代表A2和B2两种不同单质的分子,它们能反应生成新物质 X,如图是该反应的微观示意图.下列叙述正确的是( )
”分别代表A2和B2两种不同单质的分子,它们能反应生成新物质 X,如图是该反应的微观示意图.下列叙述正确的是( )
| A、X由4种元素组成 |
| B、反应过程中共出现了4种分子 |
| C、该反应为置换反应 |
| D、参加反应的A2与B2分子数之比为 3:l |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

 ”和“
”和“ ”分子个数比
”分子个数比查看答案和解析>>
科目:初中化学 来源: 题型:
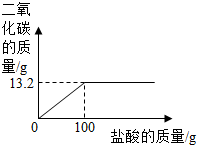 某课外兴趣小组实验测量了一定质量的碳酸钙与100g稀盐酸反应的情况,数据如图所示,计算反应后所得溶质的质量分数?(写出计算过程,结果保留到0.1%)
某课外兴趣小组实验测量了一定质量的碳酸钙与100g稀盐酸反应的情况,数据如图所示,计算反应后所得溶质的质量分数?(写出计算过程,结果保留到0.1%)查看答案和解析>>
科目:初中化学 来源: 题型:
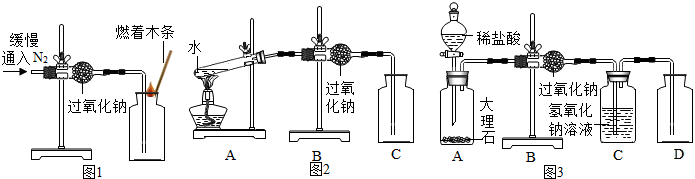
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. | A装置中观察到产生大量气泡,固体逐渐溶解.C装置中有气泡出现. | C装置作用是 |
| 打开分液漏斗活塞,向A装置中缓慢加入稀盐酸. | |||
| ② | 过氧化钠与二氧化碳反应并生成氧气. | ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、食用水产品、奶类、豆类都可以为人体补充钙元素 |
| B、硒、锌、铁、钠是人体所需的微量元素 |
| C、人体健康时胃液的pH一般在0.9~1.5范围内 |
| D、幼儿缺少碘元素,会导致智力低下,生长迟缓 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com