
【题目】根据如下装置进行碳及其氧化物的性质研究,请回答相关问题:
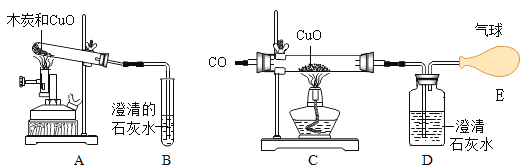
(1)图1:装置 A 中试管内木炭与氧化铜反应的现象是_____,反应的化学方程式是_____,具有还原性的物质是_____。实验结束时,立即趁热试管内固体倒在石棉网上,一段时间后,观察到 固体中又出现了黑色固体,原因是_____。
(2)图2:实验前先通一氧化碳,过点再点燃 C 处酒精灯,目的是_____,装置 C 中玻璃管内反应的化学方程式是_____。实验结束时先撤离 C 处酒精灯,待_____时停止通一氧化碳, 目的是_____。E 处加气球目的_____。
【答案】黑色固体变红 C+2CuO 2Cu+CO2↑ C 炽热的Cu与空气中的O2接触反应生成黑色CuO 排出装置中的空气,防止混合气体加热发生爆炸 CO+CuO
2Cu+CO2↑ C 炽热的Cu与空气中的O2接触反应生成黑色CuO 排出装置中的空气,防止混合气体加热发生爆炸 CO+CuO![]() Cu+CO2 装置冷却 防倒吸 吸收尾气
Cu+CO2 装置冷却 防倒吸 吸收尾气
【解析】
(1)图1:木炭和氧化铜在高温的条件下反应生成铜和二氧化碳。故装置 A 中试管内木炭与氧化铜反应的现象是:黑色固体变红,反应的化学方程式是:C+2CuO 2Cu+CO2↑,具有还原性的物质是C。实验结束时,立即趁热试管内固体倒在石棉网上,一段时间后,观察到固体中又出现了黑色固体,原因是:炽热的Cu与空气中的O2接触反应生成黑色CuO。
2Cu+CO2↑,具有还原性的物质是C。实验结束时,立即趁热试管内固体倒在石棉网上,一段时间后,观察到固体中又出现了黑色固体,原因是:炽热的Cu与空气中的O2接触反应生成黑色CuO。
(2)图2:实验前先通一氧化碳,过点再点燃 C 处酒精灯,目的是:排出装置中的空气,防止混合气体加热发生爆炸,一氧化碳与氧化铜在加热的条件下反应生成铜和二氧化碳,故装置 C 中玻璃管内反应的化学方程式是:CO+CuO![]() Cu+CO2。实验结束时先撤离 C 处酒精灯,待装置冷却时停止通一氧化碳,目的是:防倒吸。E 处加气球目的:吸收尾气,防止污染空气。
Cu+CO2。实验结束时先撤离 C 处酒精灯,待装置冷却时停止通一氧化碳,目的是:防倒吸。E 处加气球目的:吸收尾气,防止污染空气。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:初中化学 来源: 题型:
【题目】元素周期表中锌元素的某些信息如图所示,下 列有关锌的说法正确的是(____)

A 锌原子核外有30个电子
B 锌是非金属元素
C 锌的相对原子质量为65. 38g
D _____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】果糖(C6H12O6)大量存在于水果中。每个 C6H12O6 是由________个原子构成。它在体内代谢的化学方程式为:C6H12O6+6O2 ![]() 6X+6H2O,该反应生成物 X表示的物质是_______。1mol 果糖分子中碳原子的质量与______________g 蔗糖(C12H22O11)中碳原子质量相同。
6X+6H2O,该反应生成物 X表示的物质是_______。1mol 果糖分子中碳原子的质量与______________g 蔗糖(C12H22O11)中碳原子质量相同。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某碳酸钠样品中含有少量的氯化钠杂质。称取该样品25g,加人盛有足量稀盐酸的烧杯中,反应结束后气体完全逸出。反应过程中测得烧杯内混合物的质量(m)与反应时间(t)的关系如图所示。请计算:
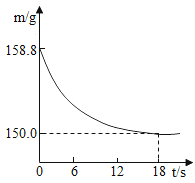
(1)完全反应后生成的CO2的质量是________g。
(2)计算样品中碳酸钠的质量分数。(写 出计算过程)______.
(3)18s末烧杯内氯化钠的质量是_________g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“化学—我们的生活,我们的未来。”
(1)“化学使天更蓝,水更清。”汽车尾气处理装置能使某些有毒气体转化为无毒气体:2NO+2CO N2+2CO2。该反应涉及的物质中,_____在空气中含量最高,_____是光合作用的原料,能与血红蛋白结合的是_____。椰子壳可加工成活性炭,用于净化空气,利用活性炭的_____性。
N2+2CO2。该反应涉及的物质中,_____在空气中含量最高,_____是光合作用的原料,能与血红蛋白结合的是_____。椰子壳可加工成活性炭,用于净化空气,利用活性炭的_____性。
(2)“化学为人类提供动力。”矿物能源有煤、_____和天然气(主要成分为甲烷/CH4),甲烷燃烧生成二氧化碳和水,其反应的化学方程式是_____。
(3)“化学为生命提供能量”。葡萄糖(C6H12O6)是生命不可缺少的物质。葡萄糖由_____种元素组成, 碳氧元素的质量比是_____,6.02×1024 个葡萄糖分子的物质的量是_____mol。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】当你参加“以水为题”的课外小组活动时,请根据以下活动内容要求,填空回答问题。
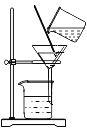
(1)从北京永定河取水样后,制成两个如下图所示的简易净水器,对河水进行初步净化。请问,简易净水器I中,用到的小卵石、石英砂和膨松棉的作用为_____(填代号),活性炭的作用为____(填代号);

A 沉淀 B 过滤 C 吸附 D 使硬水软化 E 使浑浊的水变成纯净物水
(2)使用简易净水器II处理河水时,在操作中,应沿着____慢慢向漏斗中倾倒河水,并注意液面始终要低于____。
(3)用肥皂在实验室的自来水中洗衣时,起浮渣,说明该自来水属于______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)“生命吸管”(如右图)是一种可以随身携带的小型水净化器,里面装有网丝、注入了活性炭和碘的树脂等。其中活性炭起到________和过滤的作用。
(2)水常用来配制各种溶液,硝酸钾溶液中的溶质为________。
(3)农业生产常用溶质的质量分数为10% ~ 20%的NaCl溶液来选种。现将300 g 25%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为________g。
(4)根据下表回答问题。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度 | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
①60 ℃时,向两个分别盛有50 g NaCl和NH4Cl的烧杯中,各加入100 g的水,充分溶解后,为饱和溶液的是________溶液。
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液。下列说法正确的是________(填字母序号)。
A.溶质的质量不变
B.溶液中溶质的质量分数一定减小
C.溶液质量可能不变
D.可升高温度或增加溶剂
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学将打磨过的铝箔加入到氢氧化钠溶液中,结果发现有气泡产生,为了解该气体的成分,实验小组进行了以下探究活动:
(做出猜想)
猜想一:氧气
猜想二:氢气.
猜想三:氮气.
(1)其他同学认为猜想三是错误的,理由是_____.
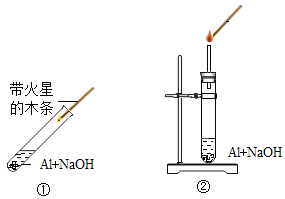
(进行实验)
分别进行实验:
(2)利用图一装置进行实验,反应一段时间后观察到_____,则猜想一错误.
(3)利用图二装置进行实验,反应一段时间,气体验纯后在尖嘴处点火.观察到_____,猜想二正确.
(得出结论)
(4)氢氧化钠、水、铝能反应,生成偏铝酸钠(NaAlO2)和氢气,请写出此反应的化学方程式_____.
(5)铝分别与足量的稀硫酸、氢氧化钠溶液反应,若生成等质量的氢气,消耗的铝的质量_____(A、硫酸多 B、氢氧化钠多 C、一样多)
(6)铝块能制成铝箔是利用了铝的_____性,铝在空气中表面形成一层致密的薄膜,具有一定的抗腐蚀性,写出相应的化学方程式_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示实验装置回答问题:
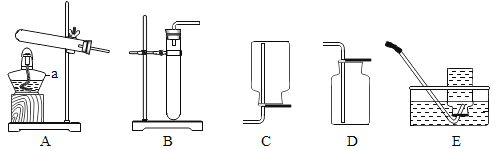
(1)图中仪器a的名称为________________;
(2)实验室用氯酸钾制取氧气,发生装置选用________________试管口应_________________;以防止____________________;
(3)若用D装置收集氧气时,检验氧气是否收集满的方法是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com