
分析处理图表中的信息是学习化学的一种重要方法.
(1)下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
Ⅰ.20℃时,NaCl的溶解度是 g/100g水.
Ⅱ.30℃时,KNO3溶 液的最大浓度(溶质质量分数)为 ; (只列计算式,不需要计算结果).
液的最大浓度(溶质质量分数)为 ; (只列计算式,不需要计算结果).
Ⅲ.从KNO3溶液中得到KNO3的一般方法是 .
Ⅳ.根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是 .
(2)如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答.
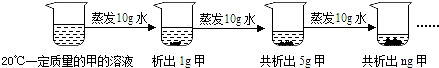
Ⅰ.蒸发前原溶液是 (填“饱和”或“不饱和”)溶液.n的数值是 .
Ⅱ.依据上述实验,你认为甲的溶解度随温度变化的趋势是 (填字母).
A.随温度升高而增大 B.随温度升高而减小 C.无法判断.
【考点】固体溶解度的影响因素;饱和溶液和不饱和溶液;饱和溶液和不饱和溶液相互转变的方法;固体溶解度的概念;溶质的质量分数、溶解性和溶解度的关系.
【专题】溶液、浊液与溶解度.
【分析】(1)根据溶解度的含义、饱和溶液时溶质质量分数最大、硝酸钾的溶解度随温度的升高而增大、KNO3和NaCl在20℃~30℃时具有相同的溶解度进行解答;
(2)根据饱和溶液的定义和判断方法进行分析;根据题中的数据以及题中析出晶体是通过蒸发溶剂得到的进行分析.
【解答】解:(1)Ⅰ.由图表可知,20℃时,NaCl的溶解度是36g/100g水;故填:36;
Ⅱ.30℃时,饱和溶液时溶质质量分数最大,30℃时,硝酸钾的溶解度为45.8g,KNO3溶液的最大浓度(溶质质量分数)为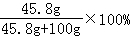 ;故填:
;故填: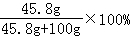 ;
;
Ⅲ.硝酸钾的溶解度随温度的升高而增大,所以从KNO3溶液中得到KNO3的一般方法是降温结晶(或冷却结晶冷却热饱和溶液);故填:降温结晶(或冷却结晶冷却热饱和溶液);
Ⅳ.根据表内数据可知,KNO3和NaCl在20℃~30℃时具有相同的溶解度,所以KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是36~36.3;故填:36~36.3;
(2)Ⅰ蒸发前的烧杯底部没有固体,第一次蒸发10g水,析出1g晶体,第二次蒸发10g水共析出5g晶体,第二次蒸发10g,析出4g晶体,所以蒸发前原溶液是不饱和溶液,第三次蒸发10g水析出4g晶体,所以共析出9g;故填:不饱和;9;
Ⅱ、题中析出晶体是通过蒸发溶剂得到的,不能判断出温度对溶解度的影响,故选:C.
【点评】解答本题关键是要知道溶解度的定义,溶解度曲线的意义,知道饱和溶液溶质质量分数的计算方法.


科目:初中化学 来源: 题型:
2010年我国纪念“世界水日”和开展“中国水周”活动的宣传主题为“严格水资源管理,保障可持续发展”.为了探究“水的净化”过程,某实验小组从九龙江中取了水样,观察到:水样呈黄色浑浊,有异味,有固体小颗粒.现对水样进行如下处理:
(1)向水样中加入明矾搅拌溶解,静置一段时间后,进行 (填操作名称),除去固体小颗粒.甲同学经过该操作处理后,水样仍浑浊,其原因可能是滤纸破损.改进操作后,滤液澄清了,再向滤液中加入活性炭,利用其 除去水样中的颜色和异味,该过程属于 变化(填“物理”或“化学”).
(2)为了判断得到的自来水是硬水还是软水,可加入 进行检验.
(3)保护水环境、珍爱水资源,是每个公民应尽的责任和义务.下列做法有利于保护水资源的是 (填序号).
A.合理使用化肥农药 B.工业废水处理达标后排放
C.使用含磷洗衣粉 D.生活污水直接排放
(4)温泉水富含钾、钙、镁、氟、硅等,这里的“钾、钙、镁、氟、硅”指的是 (填序号).
A.分子 B.原子 C.元素.
查看答案和解析>>
科目:初中化学 来源: 题型:
洁净的空气对动植物非常重要,但随着工业的发展,排放到空气中的有害气体和烟尘对空气造成污染.目前计入空气污染指数的项目暂定为: 、 、 、可吸入颗粒和臭氧等,为了保 护人类赖以生存的空气,你能做(举出一条措施) .
护人类赖以生存的空气,你能做(举出一条措施) .
查看答案和解析>>
科目:初中化学 来源: 题型:
对物质的量的理解正确的是( )
A.物质的量就是物质质量的另一种表示方式,单位是g/mol
B.物质的量就是物质的数量,数值上等于式量,单位是mol
C.物质的量就是6.02×1023个微粒的质量,单位是g
D.物质的量是国际单位制中的一个物理量,表示含有一定数目微粒的集体
查看答案和解析>>
科目:初中化学 来源: 题型:
某学习小组准备探究气体的测定和数据处理方法.
【提出问题】利用碳酸钙与稀盐酸反应来测定生成CO2的量.
【实验设计】通过下列两个实验分别测定CO2的质量和体积.

【分析处理】
实验一:
①将小烧杯中的稀盐酸分几次加入到大烧杯中,并不断搅拌,判断反应后盐酸过量的依据是 .
②若稀盐酸足量,计算理论上能产生二氧化碳的物质的量
实验二:
③先连接好装置,再 (填操作),然后装好药品,最后将20mL稀盐酸快速推入锥形瓶中.若缓慢推入,则可能造成的后果是 .
④实验记录如下(表中数据在相同温度、相同压强条件下测定):
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/mL | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
根据以上实验过程和数据综合分析,最终生成CO2的体积是 mL.
【反思与评价】
⑤经过分析,下列说法错误的是 .
A.实验一的操作简单,便于读数
B.实验一最终得到的数据和通过计算得出的理论值完全相等
C.实验二在密闭体系内反应,更环保
D.实验二中若将碳酸钙粉末改成块状的大理石,更安全.
查看答案和解析>>
科目:初中化学 来源: 题型:
学用语是学习化学的主要工具,是国际通用的化学语言.请你用相应的化学符号填空.
(1)氩气 .
(2)某气体在空气中占78%(体积百分含量),保持它的化学性质的最小粒子是.
(3)实验室常用来制取氧气的药品氯酸钾 .
(4)标出氧化铁中铁元素的化合价 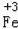 .
.
(5)到了夏天,太阳镜成为人们出行的一种常用保护工具.太阳镜是由镜脚、镜片、镜框组成.它的镜脚一般是由塑料制成的,玻璃镜片的主要成分是二氧化硅 ,且变色玻璃中含有银离子 _,铜制镜框使用时间过长会生成铜绿,铜绿中含有碳酸根离子 ﹣ .
(6)一种氮的氧化物俗称“笑气”,氮氧元素的质量比为7:4,则“笑气”为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com