
 ��ͼ��ijθҩ��ǩ�ϵIJ������ݣ�ij��ѧ��ѧ��ȤС���ͬѧ�Dzⶨ��ҩƷ��̼�����ƣ�NaHCO3��������������ȡ10Ƭ��ҩƷ���������ձ��У������ձ��еμ�ϡ������ǡ����ȫ��Ӧ�����ʲ�����ˮ��Ҳ���μӷ�Ӧ����������ϡ����23g����÷�Ӧ���ձ������ʵ�������Ϊ25.8g������㣺
��ͼ��ijθҩ��ǩ�ϵIJ������ݣ�ij��ѧ��ѧ��ȤС���ͬѧ�Dzⶨ��ҩƷ��̼�����ƣ�NaHCO3��������������ȡ10Ƭ��ҩƷ���������ձ��У������ձ��еμ�ϡ������ǡ����ȫ��Ӧ�����ʲ�����ˮ��Ҳ���μӷ�Ӧ����������ϡ����23g����÷�Ӧ���ձ������ʵ�������Ϊ25.8g������㣺���� ��1�������ձ��������ļ��������Ƕ�����̼��������
��2�����ݶ�����̼�����������̼�����Ƶ��������ٳ���ҩƷ���������ɣ�
��3�����ݶ�����̼�����������Ӧ�����ɵ������������ٳ��Է�Ӧ��������Һ���������ɣ�
��� �⣺��1��100ƬҩƷ��50g�����ÿƬ����Ϊ��$\frac{50g}{100Ƭ}$=0.5g������10ƬҩƷ������Ϊ0.5g��10=5g����Ӧ���������������Ϊ5g+23g-25.8g=2.2g��
��2����Ҫ����2.2g������̼��Ҫ�μӷ�Ӧ��̼����������ΪX�������Ȼ�������ΪY��
NaHCO3+HCl�TNaCl+H2O+CO2��
84 58.5 44
X Y 2.2g
���ݣ�$\frac{84}{X}=\frac{58.5}{Y}=\frac{44}{2.2g}$
���X=4.2g��
���Y=2.925g
ҩƷ��̼�����Ƶ���������$\frac{4.2g}{5g}$��100%=84%��
��3����Ӧ��������Һ����Ϊ��4.2g+23g-2.2g=25g����Ӧ��������Һ�����ʵ�����������$\frac{2.925g}{25g}$��100%=11.7%��
�ʴ�Ϊ����1��2.2��
��2��ҩƷ��̼�����Ƶ���������Ϊ84%��
��3����Ӧ��������Һ�����ʵ���������Ϊ11.7%��
���� �������׳����ĵط��Ƿ�Ӧ��������Һ�ļ��㣬���ʲ��ܼ��룬ֻ�ܼ�̼�����ƺ������������ټ�ȥ�����������


 ����������������ϵ�д�
����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 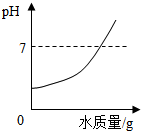 | B�� | 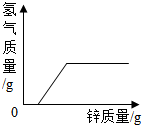 | ||
| C�� | 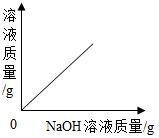 | D�� | 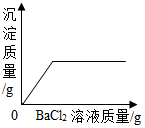 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ᡢ�������Һ�з����ķ�Ӧʵ������Һ�е�����֮��ķ�Ӧ���������Ƶ�������Ϊ��Һ���й�ͬ��H+��̼��ء�̼���Ƶ���Һ��Ҳ������ͬ�����Ӷ����ֳ����Ƶ����ʣ�����ģ�����·�ʽ�е�����һ������ʾCO${\;}_{3}^{2-}$��ijЩ��ѧ���ʣ���CO32-+H+�ѡ�����+H2O+CO2����
�ᡢ�������Һ�з����ķ�Ӧʵ������Һ�е�����֮��ķ�Ӧ���������Ƶ�������Ϊ��Һ���й�ͬ��H+��̼��ء�̼���Ƶ���Һ��Ҳ������ͬ�����Ӷ����ֳ����Ƶ����ʣ�����ģ�����·�ʽ�е�����һ������ʾCO${\;}_{3}^{2-}$��ijЩ��ѧ���ʣ���CO32-+H+�ѡ�����+H2O+CO2�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 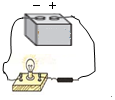 ���طŵ� | B�� |  ˮ������ | C�� |  ��ȼ��������� | D�� |  ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
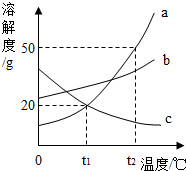 ��ͼ��a��b��c���ֹ������ʵ��ܽ�����ߣ�
��ͼ��a��b��c���ֹ������ʵ��ܽ�����ߣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com