
| 1 H +1 | 2 He 0 | ||||||
| 3 Li +1 | 4 Be +2 | 5 B +3 | 6 C +4-4 | 7 N +5-3 | 8 O -2 | 9 F -1 | 10 Ne 0 |
| 11 Na +1 | 12 Mg +2 | 13 Al +3 | 14 Si +4-4 | 15 P +5-3 | 16 S | 17 Cl +7-1 | 18 Ar 0 |
分析 根据已有的知识进行分析,钠元素属于金属元素,在化学反应中易失去电子,根据表格提供的信息可以看出,最高正价等于最外层电子数或同一列元素具有相同的化合价,He、Ne、Ar三种元素化合价为0的原因是三种元素的原子最外层电子数已达相对稳定结构.
解答 解:(1)11号元素是钠元素,属于金属元素,原子最外电子层上有1个电子,该原子易失电子,形成的钠离子与氖原子具有相同的核外电子排布,故填:1;失;Ne;
(2)16号元素为硫元素,其原子最外层有6个电子,最低负化合价为-2价,最高正合价为+6价,故氧化物的化学式为SO3;故填:-2;SO3 ;
(3)根据表格提供的信息可以看出,最高正价等于最外层电子数或同一列元素具有相同的化合价,故填:同一列元素具有相同的化合价.
(4)He、Ne、Ar三种元素化合价为0的原因是三种元素的原子最外层电子数已达相对稳定结构,故答案为:三种元素的原子最外层电子数已达相对稳定结构.
点评 本题考查了元素周期表的应用,完成此题,可以依据已有的知识进行.


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:初中化学 来源: 题型:选择题
| A. | 二氧化硫和氢氧化钠溶液 | B. | 氢氧化铜固体和稀硫酸 | ||
| C. | 硝酸银溶液和稀盐酸 | D. | 氯化钠溶液和稀盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
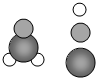 甲醛是装修材料释放出的有毒气体,其分子的模型如图所示,据此下列叙述正确的是( )
甲醛是装修材料释放出的有毒气体,其分子的模型如图所示,据此下列叙述正确的是( )| A. | 甲醛可能是氧化物 | |
| B. | 甲醛分子是由1个碳原子和1个水分子构成 | |
| C. | 甲醛中C、H、O三种元素的个数比是1:2:1 | |
| D. | 甲醛是由甲醛分子构成的纯净物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 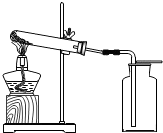 加热NH4Cl固体和熟石灰的混合物制取并收集一瓶NH3气体 | |
| B. | 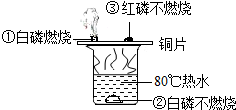 燃烧条件的实验中,热水只起隔绝氧气的作用 | |
| C. | 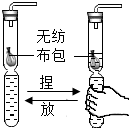 用软塑料瓶自制CO2发生装置,通过捏放瓶身可随时控制反应发生和停止 | |
| D. | 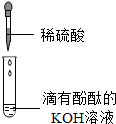 向滴有酚酞的KOH溶液中滴加稀硫酸,若反应后溶液呈无色,则恰好完全反应. |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
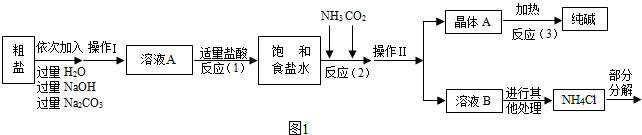
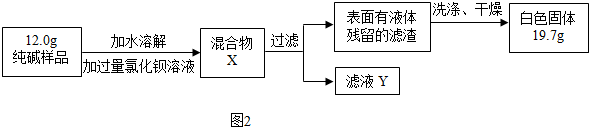
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 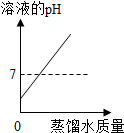 向一定量的稀盐酸中不断滴入蒸馏水 | |
| B. | 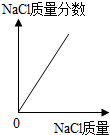 在恒定温度下,向一定量的水中不断加入氯化钠固体 | |
| C. | 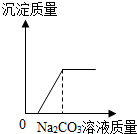 向一定量的硝酸和硝酸钙混合溶液中不断滴入碳酸钠溶液 | |
| D. | 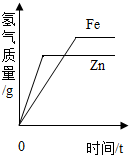 常温下过量的锌和铁分别与等量的溶质质量分数相同的稀硫酸反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com