
| A. | 20% KOH | B. | 10% KOH | C. | 20% HCl | D. | 10% HCl |
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 小明:“水是由氢元素和氧元素组成.” | |
| B. | 小红:水是由水分子构成的 | |
| C. | 小刚:水中氢、氧元素的质量比为1:8 | |
| D. | 小强:1个水分子由1个氢分子和1个氧原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生铁和钢都是铁的合金 | |
| B. | 铝比铁更耐腐蚀,所以铝比铁的活动性要弱 | |
| C. | 银的导电性比铜强,所以一般用银作电线 | |
| D. | 铁矿石在地壳中含量最丰富,可以随意开采 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
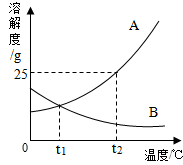
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | CaCl2溶液 | 稀盐酸 | 加过量碳酸钙,过滤 |
| B | K2CO3溶液 | KCl | 加适量稀盐酸 |
| C | CaO | CaCO3 | 加水,过滤 |
| D | NaCl溶液 | Na2CO3 | 加适量硝酸钙溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
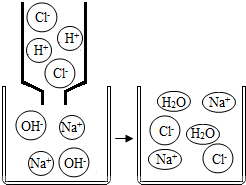 许多物质在溶液中都以离子形式存在.我们熟悉的复分解反应就是溶液中离子间结合得到水、气体或沉淀的一类化学反应.如氢氧化钠溶液与盐酸的反应就是溶液中的H+和OH-结合成水分子的过程(如图所示).结合信息,你认为下列各组离子间不能反应的是( )
许多物质在溶液中都以离子形式存在.我们熟悉的复分解反应就是溶液中离子间结合得到水、气体或沉淀的一类化学反应.如氢氧化钠溶液与盐酸的反应就是溶液中的H+和OH-结合成水分子的过程(如图所示).结合信息,你认为下列各组离子间不能反应的是( )| A. | H+ Na+ OH- NO3- | B. | Ca2+ K+ Cl- NO3- | ||
| C. | H+ Na+ CO32- HCO3- | D. | K+ Ba2+ Cl- SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com