
| A. | K+、OH-、NO3- | B. | K+、Na+、SO42- | C. | Ca2+.CO32-、Cl- | D. | NH4+、Cu2+、Cl- |
分析 pH为2的水溶液显酸性,水溶液中含有大量的H+;根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能共存.本题还要注意溶液呈无色,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:A、在pH=2的无色溶液中,H+和OH-能结合生成水,则不能大量共存,故选项错误;
B、在pH=2的无色溶液中,三种离子不能结合生成水、气体、沉淀,则能大量共存,故选项正确;
C、在pH=2的无色溶液中,H+和CO32-能结合生成水和二氧化碳气体,Ca2+和CO32-能结合生成碳酸钙沉淀,则不能大量共存,故选项错误;
D、因Cu2+在溶液中为蓝色,则与无色溶液相矛盾,故选项错误;
故选B.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水;解题时要注意酸性溶液中中含有大量的H+.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题

| 实验 | 30%双氧水的质量(g) | 加入的水体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 提倡步行、騎自行车等“低碳”出行方式 | |
| B. | 通过加髙烟囱排除放工业废气 | |
| C. | 鼓励用农作物秸秆做燃料 | |
| D. | 施用大量的化肥和农药以提高农作物产量 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  向饱和KNO3溶液中加入KNO3 | |
| B. | 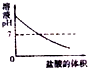 向NaOH溶液中滴加盐酸至过量 | |
| C. |  向CuCl2和HCl的混合溶液中加入加量NaOH溶液 | |
| D. |  向两份同体积和同质量分数的HCl溶液中分别加入足量的铁粉和镁粉 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图所示,请回答下列问题:
如图所示,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

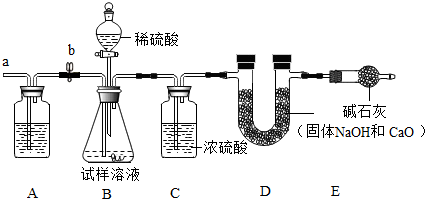
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com