
| 物质(纯净物) | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 2.3 | 4 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 2.2 | 2.7 | 待测 |
| A. | 反应后X的质量为1.4g | B. | X中一定含有碳元素和氢元素 | ||
| C. | X中一定含有碳元素和氧元素 | D. | X中两种元素的质量比为1:1 |
分析 根据质量守恒定律分析,根据表中的数据确定反应物、生成物.反应后质量减少的物质是反应物,质量增加的物质是生成物.通过计算乙醇、氧气、二氧化碳、水中各元素的质量,根据质量守恒定律可以确定X的组成、质量和化学式;经计算知X是一氧化碳,说明乙醇没有充分燃烧,增加氧气的量有助于乙醇的充分燃烧,从而减少一氧化碳的生成.
解答 解:由表中数据分析可知,反应前后乙醇的质量减少了2.3g-0g=2.3g,故乙醇是反应物,参加反应的乙醇的质量为2.3g;同理可以确定氧气是反应物,参加反应的氧气的质量为4g-0g=4g;二氧化碳是生成物,生成的二氧化碳的质量为2.2g-0g=2.2g;水是生成物,生成的水的质量为:2.7g-0g=2.7g;由质量守恒定律,X是生成物,且生成X的质量为2.3g+4g-2.2g-2.7g=1.4g,故待测的数值为1.4g-0g=1.4g.
A、由以上分析可知,反应后X的质量为1.4g,故选项说法正确.
B、由化合物中某元素的质量=化合物的质量×化合物中该元素的质量分数可以计算出:2.3g乙醇中碳、氢、氧三元素的质量分别是1.2g、0.3g、0.8g;2.2g二氧化碳中碳、氧两元素的质量分别是0.6g、1.6g;2.7g水中氢、氧两元素的质量分别为0.3g、2.4g.因此反应物中共有1.2g碳元素、0.3g氢元素、4.8g氧元素,生成物二氧化碳和水中共有0.6g碳元素、0.3g氢元素、4g氧元素.根据质量守恒定律可知:反应物中有0.6g碳元素和0.8g氧元素进入了生成物X中,说明生成物X由碳、氧两元素组成,X中不含氢元素,故选项说法不正确.
C、根据B选项的分析,物质X一定含有碳元素和氧元素,故选项说法正确.
D、根据B选项的分析,可知生成物X中碳元素和氧元素的质量比为:0.6g:0.8g=3:4;故选项说法不正确.
故选AC.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:初中化学 来源: 题型:填空题
 ”表示氧原子,“
”表示氧原子,“ ”表示氢原子,“
”表示氢原子,“ ”表示氯原子)
”表示氯原子)
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
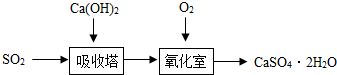 我国大气污染的主要来源是生产和生活使用化石燃料.燃煤等,SO2是主要大气污染物之一,用石灰浆吸收SO2转化为石膏是一种工业上烟气脱硫的方法如图:
我国大气污染的主要来源是生产和生活使用化石燃料.燃煤等,SO2是主要大气污染物之一,用石灰浆吸收SO2转化为石膏是一种工业上烟气脱硫的方法如图:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 干冰升华需吸收大量的热,可用于人工降雨 | |
| B. | Ca(OH)2能与酸反应,可用于改良酸性土壤 | |
| C. | 用武德合金制作保险丝,是因为熔点低 | |
| D. | 明矾溶于水能形成吸附性物质,可用于自来水厂杀菌消毒 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是有关盐酸的知识网络图,用化学用语回答:
如图是有关盐酸的知识网络图,用化学用语回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
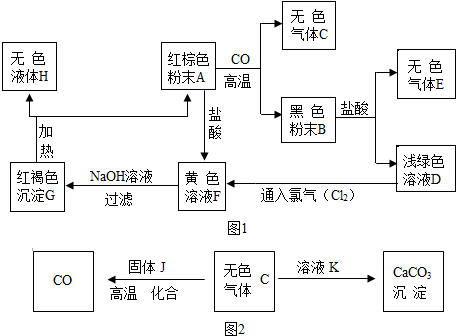
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
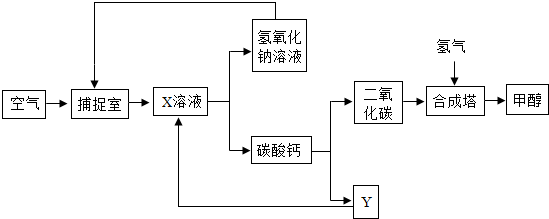
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 人类社会的可持续发展离不开能源和新型材料.
人类社会的可持续发展离不开能源和新型材料.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com