
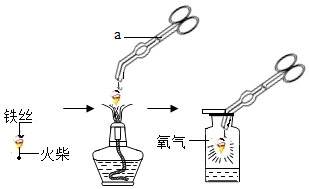
 实验是研究化学的基本手段.在实验室,小冬同学进行了“铁在氧气中燃烧”的实验,请回答下列问题:
实验是研究化学的基本手段.在实验室,小冬同学进行了“铁在氧气中燃烧”的实验,请回答下列问题:| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
根据实验中火柴的作用是:引燃铁丝;铁和氧气在点燃的条件下生成四氧化三铁;集气瓶中装少量水的目的是:防止溅落的熔化物炸裂瓶底进行分析;
(2)首先根据铁能与稀盐酸反应生成气体,也能与硫酸铜反应,置换出红色的铜,来鉴别黑色物质中是否含有铁;再根据实验条件,控制温度,以制取Fe3O4;最后,在集气瓶底部放少量的水或沙子,就能防止热的固体溅落炸裂集气瓶;已知反应物和生成物,写出反应,配平即可;如果包装盒破损进气,空气中的氧气就把氧化亚铁氧化,黑色就变成红棕色氧化铁.
解答 解:(1)通过分析题中所指仪器的作用可知,a是坩埚钳,实验中火柴的作用是:引燃铁丝;铁和氧气在点燃的条件下生成四氧化三铁,化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,集气瓶中装少量水的目的是:防止溅落的熔化物炸裂瓶底;
(2):【实验探究】部分:要想证明,铁燃烧时溅落下来的黑色物质中还含有铁,可以将冷却后的黑色物质碾碎,装入试管,加入稀盐酸或硫酸铜等溶液,如果出现冒气泡、生成红色固体等现象,就证明黑色物质中还含有铁.
【理论探讨】根据Fe3O4和Fe2O3的分解温度、铁的熔点,首先铁需要在融化状态下反应,所以应该是高于1535℃,其次是要防止四氧化三铁分解,所以温度应该是低于1538℃,所以应该控制温度在l535℃~l538℃,这时Fe2O3的分解温度低,已经分解了,铁在氧气里燃烧的产生是只有Fe3O4;
【拓展延伸】(1)氧化铁在高温的条件下生成四氧化三铁和氧气,化学方程式为:6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑;
(2)如果包装盒破损进气,空气中的氧气就把氧化亚铁氧化,黑色就变成红棕色氧化铁.
故答案为:(1)坩埚钳,引燃铁丝;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,防止溅落的熔化物炸裂瓶底;
(2)【实验探究】稀盐酸、硫酸铜等;冒气泡、生成红色固体等;
【理论探讨】l535℃~l538℃;
【拓展延伸】
(1)6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+O2↑;
(2)红色.
点评 本题考查铁的化学性质,探究铁的不同氧化物之间的转化关系,以及控制反应条件得到不同产物的方法.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
 用右如图装置加热高锰酸钾制取氧气,指出装置中的三处错误:导气管插入试管太长、试管口向上倾斜、试管口没有棉花.
用右如图装置加热高锰酸钾制取氧气,指出装置中的三处错误:导气管插入试管太长、试管口向上倾斜、试管口没有棉花.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
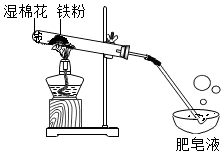 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 能否与盐酸反应 | 能 | 能 | 能 |
| 实验操作 | 实验现象及结论 |
| 取少量黑色固体于试管中,加入足量的稀盐酸. | 若固体不溶解,也没有气泡冒出,剩余固体是Fe3O4.若固体部分溶解,有气泡冒出,剩余固体是Fe与Fe3O4. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
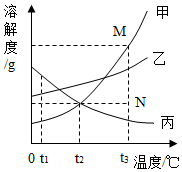 图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述错误的是( )
图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述错误的是( )| A. | t2℃时,三种物质的溶解度大小顺序为:乙>甲=丙 | |
| B. | t2℃时,甲、丙两种物质的溶液中溶质的质量分数相等 | |
| C. | 若甲物质中混有少量的乙物质,可用降温结晶的方法提纯甲 | |
| D. | 采用降低温度的方法,可将饱和的丙物质溶液变成不饱和 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
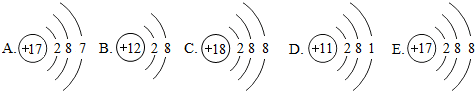
| A. | 同种分子构成的物质一定是纯净物,所以纯净物一定由同种分子构成 | |
| B. | 同种元素质子数相同,所以质子数相同的粒子统称同种元素 | |
| C. | 物质和氧气发生的反应是氧化反应,所以发生氧化反应一定有氧气参加 | |
| D. | 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com