
| A. | 1g | B. | 1.6g | C. | 2g | D. | 8.5g |
分析 过氧化氢溶液有H2O和H2O2,根据氢氧元素质量比可以算出过氧化氢的含量,然后根据氢元素的质量守恒就可以算出生成氧气的质量.
解答 解:某H2O2溶液中H、O的质量比为2:17;
则:38g双氧水溶液中氢元素质量为:38g×$\frac{2}{2+17}$=4g
根据过氧化氢分解的化学方程式可以知道,过氧化氢完全反应后生成水和氧气,该过程中氢元素的质量没有改变;所以反应后水的质量为:4g÷$\frac{1×2}{1×2+16}$×100%=36g
所以根据质量守恒定律可以知道生成氧气的质量为 38g-36g=2g;
故选C.
点评 该考点的命题方向主要是通过创设相关问题情景或图表信息等,来考查学生对根据化学反应方程式的计算步骤和格式的理解和掌握情况,要想解答好这类题目,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等,有时候如果能正确的运用元素守恒的思想来解答相关问题能起到事半功倍的效果.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 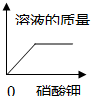 一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 | |
| B. | 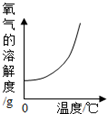 在一定条件下,氧气的溶解度随温度的变化 | |
| C. |  向盐酸和氯化镁的混合溶液中滴加氢氧化钾溶液 | |
| D. |  该反应是NaOH溶液滴入稀HCl中 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验一 | 实验二 | 实验三 | |
实验 方案 |  |  |  |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色. | 无现象 | 铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | 铝能和稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是② | |||
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | +4 | B. | -4 | C. | +2 | D. | +6 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①②⑤ | C. | ①③④ | D. | ③⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 氯化钙钾石的化学式为KCl•xCaC12(x是CaCl2的系数).它是一种天然的钾肥,溶于水后得到KCl与CaCl2的混合溶液.某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解得到KCl与CaCl2的混合溶液,向该溶液中逐滴加入Na2CO3溶液,产生的沉淀与加入Na2CO3溶液的质量关系如图所示.请回答下列问题:
氯化钙钾石的化学式为KCl•xCaC12(x是CaCl2的系数).它是一种天然的钾肥,溶于水后得到KCl与CaCl2的混合溶液.某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解得到KCl与CaCl2的混合溶液,向该溶液中逐滴加入Na2CO3溶液,产生的沉淀与加入Na2CO3溶液的质量关系如图所示.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com