
某碳酸钠样品中含有少量氯化钠杂质。现将一定量样品放入烧杯中,称得总质量为163.9g,加入146.1g氯化钙溶液,恰好完全反应,产生沉淀10g,过滤后,所得溶液中溶质的质量分数为10%,计算样品中Na2CO3的质量分数?
(反应方程式为:Na2CO3 +CaCl2 === 2NaCl + CaCO3↓)
解:设样品中NaCl的质量为m,样品中Na2CO3的质量为x,生成的
NaCl的质量为y
Na2CO3 + CaCl2 = 2NaCl + CaCO3↓
106 117 100
x y 10g
|

 |
|
 ---------------1分
---------------1分
10.6g + m + 146.1g – 10g = (11.7g +m) ÷ 10%
m= 3.3g ---------------1分
 ---------------1分
---------------1分
答:样品中Na2CO3的质量分数为76.3%。
【解析】已知产生的10克沉淀就是碳酸钙,据此根据化学反应方程式即可计算了具体步骤见答案。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:阅读理解
 水是重要的资源,是人及一切生物生存所必需的,自然界的水含有各种杂质,很少能直接使用,须进行净化.
水是重要的资源,是人及一切生物生存所必需的,自然界的水含有各种杂质,很少能直接使用,须进行净化.查看答案和解析>>
科目:初中化学 来源: 题型:
 ?
?| 实验步骤 | 实验现象 |
| 在混合液中加入过量的氯化钙溶液,充分反应后过滤,得到澄清溶液 | 产生白色沉淀 |
| 所得滤液中的溶质是: CaCl2、NaOH CaCl2、NaOH 填化学式) | |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
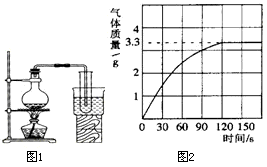 水是重要的资源,是人及一切生物生存所必需的,自然界的水含有各种杂质,很少能直接使用,须进行净化.
水是重要的资源,是人及一切生物生存所必需的,自然界的水含有各种杂质,很少能直接使用,须进行净化.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 实验步骤 | 实验现象 |
| 在混合液中加入过量的氯化钙溶液,充分反应后过滤,得到澄清溶液 | 产生白色沉淀 |
| 所得滤液中的溶质是:______填化学式) | |
查看答案和解析>>
科目:初中化学 来源:2012年江苏省镇江市索普实验学校中考化学模拟试卷(8)(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com